Química

Químico e físico francês, Joseph Louis Gay-Lussac nasceu em Saint-Léonard-de-Noblat, a 6 de dezembro de 1778, e faleceu em Paris a 9 de maio de 1850. Estudou na École Polytechnique, onde foi discípulo de Berthollet. Em 1809 assumiu a cadeira de química da École Polytechnique e a de física da Sorbonne.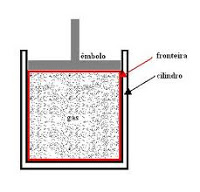
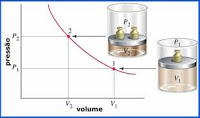
A Lei de Gay-Lussac que abrange tanto a Química e a Física é a lei dos gases perfeitos: sob volume constante, a pressão de um gás aumenta proporcionalmente com a temperatura. A fórmula pra calcular este princípio é a seguinte:
- A Presença Dos Gases No Nosso Dia A Dia
Bolsista: Roniel Francisco Olá pessoal do quipibid, hoje vamos falar sobre um assunto do nosso cotidiano; eles estão por toda parte, não podem ser vistos, mas, podemos sentir sua presença e fazer diversas experiências com eles.Vamos conhecer um pouco...
- Avogadro E A Teoria AtÔmico-molecular
Bolsista: Walmira Gomes Olá pessoal do Quipibid, estamos de volta com as nossas colunas, atualizadas e com novidades!Vamos falar sobre as contribuições de Avogadro para a Teoria atômico-molecular e para a evolução da química.Amedeo di Quarema Avogadro...
- Robert Boyle
Bolsista: Leidiane R. RosaCélebre pelas pesquisas que realizou no campo da física, da química e das ciências naturais, Robert Boyle nasceu em Lismore Castrle em Munster, Irlanda, em 25 de Janeiro de 1627 , começou a estudar latim e francês com...
- Avogadro - A Sua ContribuiÇÃo Para A QuÍmica
Bolsista: Leidiane R. Rosa Químico e físico italiano, Amedeo Avogadro, nasceu em Turim, em 9 de agosto de 1776, e faleceu em 9 de julho de 1856. Foi Conde de Quarequa e de Cerreto herdou o título de nobreza do pai, também foi presidente...
- Antoine César Becquerel
Antoine César Becquerel (Châtillon-Coligny, 7 de março de 1788 ? Châtillon-sur-Loing, 18 de janeiro de 1878) foi um físico francês. Descobridor da célula fotovoltaica (1839) é considerado o pai da eletroquímica. Entrou na École Polytechnique...
Química
Gay-Lussac
Bolsista: Leidiane Rosa

É conhecido atualmente pelas contribuições que fez às leis dos gases. Em 1802, Gay-Lussac foi o primeiro a formular a segunda lei dos gases, que se pode enunciar da seguinte forma: Quando se mantém a pressão constante, o volume de um gás é diretamente proporcional à sua temperatura absoluta. Esta lei é conhecida atualmente como Lei de Charles e Gay-Lussac.

Outra grande contribuição de Gay-Lussac é a sua Lei volumétrica, onde ele afirma que nas mesmas condições de temperatura e pressão, o volume resultante da combinação de dois gases mantém uma relação numérica simples com os volumes de cada um deles, sua tese foi publicada em 1808, e envolvia a reação entre o hidrogênio e oxigênio, cujo produto era vapor de água. Esse princípio, conhecido como lei das combinações simples ou lei de Gay-Lussac, contribuiu decisivamente para o estabelecimento da hipótese de Avogadro.
Em 1804, fez duas ascensões em balão, com o objetivo de estudar as regiões elevadas da atmosfera. Suas investigações científicas foram com êxito, havendo, entre outros importantes resultados, averiguado a invariabilidade da composição do ar e as variações do campo magnético em função da altitude.
Em companhia de Thénard, Gay-Lussac isolou o potássio, em 1808, extraindo-o da potassa fundida, em 1805 determinou com bastante precisão a composição volumétrica da água; em 1808 isolou o boro; em 1815 isolou o cianogênio e, no ano seguinte, determinou a composição do peróxido de nitrogênio.
Por sua notável contribuição para o progresso da química, foi eleito para Academie de Sciences, de Paris, e para a Royal Society, de Londres.

P=K
T
Onde: P é a pressão do gás
T é a temperatura do gás (em Kelvin)
K é uma constante
Referencias
www.explicatorium.com/Joseph-Gay-Lussac.php
allchemy.iq.usp.br/metabolizando/beta/01/gay.htm
http://www.mundoeducacao.com.br/quimica/leis-gay-lussac.htm
loading...
- A Presença Dos Gases No Nosso Dia A Dia
Bolsista: Roniel Francisco Olá pessoal do quipibid, hoje vamos falar sobre um assunto do nosso cotidiano; eles estão por toda parte, não podem ser vistos, mas, podemos sentir sua presença e fazer diversas experiências com eles.Vamos conhecer um pouco...
- Avogadro E A Teoria AtÔmico-molecular
Bolsista: Walmira Gomes Olá pessoal do Quipibid, estamos de volta com as nossas colunas, atualizadas e com novidades!Vamos falar sobre as contribuições de Avogadro para a Teoria atômico-molecular e para a evolução da química.Amedeo di Quarema Avogadro...
- Robert Boyle
Bolsista: Leidiane R. RosaCélebre pelas pesquisas que realizou no campo da física, da química e das ciências naturais, Robert Boyle nasceu em Lismore Castrle em Munster, Irlanda, em 25 de Janeiro de 1627 , começou a estudar latim e francês com...
- Avogadro - A Sua ContribuiÇÃo Para A QuÍmica
Bolsista: Leidiane R. Rosa Químico e físico italiano, Amedeo Avogadro, nasceu em Turim, em 9 de agosto de 1776, e faleceu em 9 de julho de 1856. Foi Conde de Quarequa e de Cerreto herdou o título de nobreza do pai, também foi presidente...
- Antoine César Becquerel
Antoine César Becquerel (Châtillon-Coligny, 7 de março de 1788 ? Châtillon-sur-Loing, 18 de janeiro de 1878) foi um físico francês. Descobridor da célula fotovoltaica (1839) é considerado o pai da eletroquímica. Entrou na École Polytechnique...
