Química
- Questões 1a Série Caderno Do Aluno Vol.1
...
- A Gasolina!
Bolsista: Tatiane dos Santos Ferreira Olá amigos do QUIPIBID! Venho hoje trazer uma matéria sobre um combustível muito utilizado por nós: A Gasolina! Vocês sabiam que a gasolina é o segundo combustível mais consumido no Brasil,...
- Colocando Fogo Em Dinheiro
Adaptação: Solange Batista de Sousa Anacleto ReisMATERIAIS NECESSÁRIOS 50 mL de álcool isopropílico 50 mL de água destilada Bécker de 1 litro ou...
- Questões De Termoquímica E Balanceamento. Resolvidas
2) A queima de 4,6 g de álcool libera 32,6 Kcal. Sabendo que a densidade do álcool é de 0,8 g/ml, qual é o calor liberado na queima de 1 litro de álcool? 1 litro de álcool possui massa de 800 gPortanto:4,6 g de álcool .................32,6 Kcal800...
- Hidrocarbonetos E Álcoois - Avaliação Da Aprendizagem
I) Monte a F.E dos compostos orgânicos:1. Etano2. Pent-2-eno3. But-1-ino4. Ciclopropano5. ...
Química
O ÁLCOOL DO NOSSO DIA A DIA
| Tatiane dos Santos |
Olá amigos do blog!
O assunto de hoje é bastante conhecido por todos, o álcool ou quimicamente falando etanol, ou melhor, álcool etílico!
O etanol é um composto orgânico obtido na maioria das vezes da cana de açúcar, porém outros vegetais ricos em amido como: mandioca, milho entre outros também podem ser utilizados para produzir etanol. Este é muito utilizado na indústria na fabricação de bebidas alcoólicas, perfumes, produtos de limpeza, combustível e etc. O processo utilizado para se obter essa matéria prima é chamado de fermentação.
A fermentação é um processo de liberação de energia anaeróbio (ocorre sem a presença do gás oxigênio). São adicionados micro organismos ao caldo da cana que rompem as moléculas de açúcar (C6H12O6) presentes na matéria transformando-as em duas moléculas de etanol e duas de gás carbônico, como podemos observar na reação abaixo:
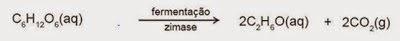
Fatores como a acidez e a temperatura devem ser controlados, logo o meio deve ser ácido e a temperatura por volta de 28ºC. Este processo dura aproximadamente 50 h e a quantidade de álcool obtido é por volta de 13% do volume do suco em fermentação. É claro que estes dois fatores dependem dos vegetais utilizados.
Ao fim da fermentação, ocorre o processo de destilação fracionada, onde se separa o álcool do sumo fermentado e se obtém frações de composições diferentes, sendo uma delas uma mistura de 96% de álcool e 4% de água, conhecido como álcool 96º GL, ou seja, 96 graus Gay-Lussac. Para se obter álcool puro, anidro ou absoluto, deve-se retirar a água presente no álcool.
Ø Podemos citar algumas características químicas do etanol:
Formula Molecular: CH3CH2OH
Ponto de Fusão: - 115º C
Ponto de Ebulição: 78º C
pH: Neutro
Poder Calorífico: 5,380 (kcal/l)
Ø Curiosidade (Etanol x Gasolina)
Será que a Gasolina rende mais que o etanol?
SIM, pois o potencial enérgico da gasolina é maior que o do álcool, enquanto o poder calorífico (quantidade de energia que um combustível gera em sua queima dentro do motor) do álcool é de 5,380 (kcal/l) o da gasolina é 8,325 (Kcal/l). O litro da gasolina chega a fazer 30% a mais que 1 litro do álcool.
Fiquem ligados meus amigos, nos vemos na próxima, onde vamos continuar falando dos combustíveis! O próximo será a GASOLINA!
Referências:
NOBREGA. O. S.; SILVA. E, R, da; SILVA. R, H, da QUÍMICA Volume único. Ed. Ática. São Paulo, 2007.
NOVA CANA. Disponível em: <http://www.novacana.com/etanol/propriedades-fisico-quimicas/> acesso: 13 de Abril de 2015.
loading...
- Questões 1a Série Caderno Do Aluno Vol.1
...
- A Gasolina!
Bolsista: Tatiane dos Santos Ferreira Olá amigos do QUIPIBID! Venho hoje trazer uma matéria sobre um combustível muito utilizado por nós: A Gasolina! Vocês sabiam que a gasolina é o segundo combustível mais consumido no Brasil,...
- Colocando Fogo Em Dinheiro
Adaptação: Solange Batista de Sousa Anacleto ReisMATERIAIS NECESSÁRIOS 50 mL de álcool isopropílico 50 mL de água destilada Bécker de 1 litro ou...
- Questões De Termoquímica E Balanceamento. Resolvidas
2) A queima de 4,6 g de álcool libera 32,6 Kcal. Sabendo que a densidade do álcool é de 0,8 g/ml, qual é o calor liberado na queima de 1 litro de álcool? 1 litro de álcool possui massa de 800 gPortanto:4,6 g de álcool .................32,6 Kcal800...
- Hidrocarbonetos E Álcoois - Avaliação Da Aprendizagem
I) Monte a F.E dos compostos orgânicos:1. Etano2. Pent-2-eno3. But-1-ino4. Ciclopropano5. ...
