Química
Para muitas reações químicas o uso de um catalisador é necessário, com a finalidade de obter uma reação química com maior velocidade.
- Balanceamento Químico
Balanceamento Das Equações Químicas Para as primeiras séries do ensino médio. A Definição de...
- Garrafa Azul
Bolsista: Solange Batista de Sousa Anacleto ReisMATERIAIS UTILIZADOS 180 mL de água destilada; 3,5 g de NaOH (hidróxido de sódio), a popular soda cáustica; 6 g de C6H12O6(glicose),...
- Termoquímica
Termoquímica é a parte da Química que estuda as quantidades de calor liberadas ou absorvidas durante as reações químicas.Os calores liberados ou absorvidos pelas reações são expressos em Joule (J), ou caloria (cal). Imagem: Química Ensinada...
- Luminol
A reação de quimiluminescência do luminol é responsável pelo brilho de lightsticks. A reação é usada por criminalistas para detectar vestígios de sangue em cenas de crime. Neste teste, o luminol em pó (C 8 H 7 O 3 N 3 ) é misturado com peróxido...
- Creme Dental De Elefante
Observe neste vídeo a Decomposição do Peróxido de Hidrogênio. O experimento também é conhecido como Creme Dental de Elefante. Importante: Caso resolva experimentar, cuidado! Sempre faça com conhecimento prévio. Não faça experimentos químicos...
Química
Decomposição de Peróxido de Hidrogênio, com auxílio de catalisador (Lâmpada Mágica)
Decomposição de H2O2, com auxílio de catalisador
Para muitas reações químicas o uso de um catalisador é necessário, com a finalidade de obter uma reação química com maior velocidade.
No vídeo foi demonstrado a reação de decomposição da água oxigenada a 30%, utilizando-se como catalisador o MnO2 .
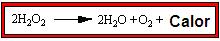
A reação química acontece de forma vigorosa e exotérmica. Esta reação libera água, oxigênio e calor, como mostrado na equação.
Sem o catalisador MnO2, essa reação não ocorreria a um ritmo apreciável. Esta é uma reação muito visual, podendo ser realizada também dentro de uma garrafa PET de 2L.
Esta reação pode ser relacionada a muitas observações de nosso cotidiano. Como no caso dos catalisadores em sistemas de exaustão de automóveis (escapamentos), onde também são empregados catalisadores, tendo como uma das finalidades a diminuição da emissão de poluentes.
Para a realização do experimento de decomposição da H2O2 com MnO2, vamos precisar:
Observação: A reação é exotérmica, oferece riscos, não faça em casa, não faça sem o acompanhamento de um profissional habilitado, enfim, tome cuidado. Química Ensinada Recomenda!!!
Materiais:
Peróxido de hidrogênio (H2O2) 30%
Dióxido de manganês MnO2
Pilão
Limpe duas garrafas de PET.
Procedimento:
Como descrito no vídeo.
Cuidado.
?
loading...
- Balanceamento Químico
Balanceamento Das Equações Químicas Para as primeiras séries do ensino médio. A Definição de...
- Garrafa Azul
Bolsista: Solange Batista de Sousa Anacleto ReisMATERIAIS UTILIZADOS 180 mL de água destilada; 3,5 g de NaOH (hidróxido de sódio), a popular soda cáustica; 6 g de C6H12O6(glicose),...
- Termoquímica
Termoquímica é a parte da Química que estuda as quantidades de calor liberadas ou absorvidas durante as reações químicas.Os calores liberados ou absorvidos pelas reações são expressos em Joule (J), ou caloria (cal). Imagem: Química Ensinada...
- Luminol
A reação de quimiluminescência do luminol é responsável pelo brilho de lightsticks. A reação é usada por criminalistas para detectar vestígios de sangue em cenas de crime. Neste teste, o luminol em pó (C 8 H 7 O 3 N 3 ) é misturado com peróxido...
- Creme Dental De Elefante
Observe neste vídeo a Decomposição do Peróxido de Hidrogênio. O experimento também é conhecido como Creme Dental de Elefante. Importante: Caso resolva experimentar, cuidado! Sempre faça com conhecimento prévio. Não faça experimentos químicos...
