Química
Olha pessoal! Mas uma vez estou com vocês, para levar algumas informações sobre mais um ?Elemento Químico?. Hoje vamos conhecer um pouquinho do Fósforo (P), um elemento bastante conhecido e com várias utilizações em diversas áreas. O fósforo é um elemento sólido à temperatura ambiente. O fósforo branco é mole, de aspecto ceroso, e bastante reativo. Reage com ar úmido desprendendo luz (quimioluminescência). Ele se inflama espontaneamente no ar a cerca de 35 º C, sendo armazenado sob água para impedir essa reação. É extramente tóxico, podendo ser encontrado na forma de moléculas P4tetraédricas. Essa estrutura é mantida nos estados líquido e gasoso. Acima de 800 ºC, as moléculas de P4 gasosos começaram a se dissociar formando P2, que possuem uma energia de ligação de 489,6 KJ mol -1(este corresponde somente à metade do valor para o N2, pois os orbitais do terceiro nível são muito maiores, sendo a interação p?- p? relativamente fraca).

- Gadolínio (gd)
Bolsista:...
- Protactínio (pa)
Bolsista:Leonice Paraguai Olha pessoal! Vamos conhecer mais um ?Elemento Químico?. O elemento de hoje é o Protactínio (Pa), o protactínio não tem aplicações práticas. As pequenas quantidades de Protactínio é cerca de o, 1 ppm de 231 Pa, são...
- Samário (sm)
...
- Àcido Fosfórico
...
- Arsênio (as)
Bolsista: Leonice ParaguaiOlha pessoal! Estou de volta novamente, para falar um pouco mais de outro ?Elemento Químico?. Hoje vou falar do Arsênio (As), que é um elemento usado desde antiguidade. Os efeitos tóxicos e muitas vezes letais do arsênio,...
Química
Fósforo (P)
Bolsista: Leonice Paraguai

Se o fósforo branco for aquecido a cerca de 250 º C, ou a uma temperatura menor na presença de luz solar, forma-se o fósforo vermelho. Trata-se de um sólido polimérico, muito menos reativo que o fósforo branco. É estável ao ar e não sofre ignição, a não ser mediante aquecimento a 400 ºC. Não é necessário armazená-la sob água. É insolúvel em solventes orgânicos. Uma forma altamente polimerizada de fósforo denominada fósforo preto pode ser obtido aquecendo-se o fósforo branco, a pressões elevadas. Essa é a forma alotrópica termodinamicamente mais estável. É inerte e apresenta uma estrutura lamelar. Ver a figura.
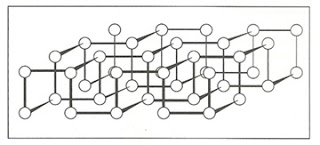 |
A estrutura do fósforo preto. No fósforo preto cristalino, os átomos estão dispostos em planos dobrados. O uso dos fosfatados nos fertilizante, as rochas fosfáticas, como a fluorapatita, [3 Ca3 (PO4)2 CaF2], são pouco solúveis e, portanto, não estão disponíveis para as plantas. O ?superfosfato? é preparado, tratando-se as rochas fosfáticas com H2 SO4 concentrado. O sal ácido Ca (H2PO4)2é mais solúveis e o superfosfato se dissolverá na água do solo no período de algumas semanas. Superfosfato O CaSO4 é um subproduto insolúvel sem valor para as plantas, mas não é removido do produto comercializado. O ?superfosfato triplo? é fabricado de maneira semelhante, usado H3PO4 para evitar a formação do subproduto CaSO4. Superfosfato triplo Os fosfatos são detectados analiticamente, misturando-se uma solução do sal com HNO3 diluído e solução de molibdado de amônio. Forma-se lentamente um precipitado amarelo de 12-molibdofosfato de amônio. Bom pessoal! Estarei de volta na próxima semana com mais um ?Elemento Químico?. Uma ótima semana para todos e lembre-se você sozinho não é capaz de mudar o mundo, mas se você fizer sua parte, estará contribuindo para um mundo melhor. Referência: Lee, J. D. Química inorgânica não tão concisa, 5ª ed. São Paulo: Blucher, P.239. 248. 249. 257. 1999. |
loading...
- Gadolínio (gd)
Bolsista:...
- Protactínio (pa)
Bolsista:Leonice Paraguai Olha pessoal! Vamos conhecer mais um ?Elemento Químico?. O elemento de hoje é o Protactínio (Pa), o protactínio não tem aplicações práticas. As pequenas quantidades de Protactínio é cerca de o, 1 ppm de 231 Pa, são...
- Samário (sm)
...
- Àcido Fosfórico
...
- Arsênio (as)
Bolsista: Leonice ParaguaiOlha pessoal! Estou de volta novamente, para falar um pouco mais de outro ?Elemento Químico?. Hoje vou falar do Arsênio (As), que é um elemento usado desde antiguidade. Os efeitos tóxicos e muitas vezes letais do arsênio,...
