Química
Soluções
Soluções diluídas
A quantidade de soluto dissolvido é pequena. Exemplo os sais presentes na água mineral que tomamos.
Uma solução de hidróxido de sódio NaOH) 0,02 molar é uma solução diluída.
Uma solução de ácido clorídrico (0,01) molar é uma solução diluída.
Exemplos de Algumas Soluções
Solução de ácido bórico H3BO3.
Quando seco é um Cristal sólido pó incolor ou branco - o solvente é a água, 100 mL de água dissolve 5,14 g desse ácido.
Solução de bicromato de potássio K2Cr2O7 apresenta-se sólido, na forma de cristal - solvente água, dissolve-se 147 g dessa substância em água e completa-se para um litro. Para vários usos, determinação quantitativa de molibdênio, ou para lavagem de instrumentos que se exige certa assepsia, também é utilizado na determinação quantitativa de glicerina.
Soluções Concentradas
O soluto está dissolvido completamente até o seu limite de dissolução no solvente.
Uma solução de hidróxido de sódio (NaOH) 4 molar é uma solução concentrada.
Uma solução de ácido clorídrico (HCl) 4 molar é uma solução concentrada.
Soluções Saturadas
A quantidade do soluto presente na solução ultrapassou o limite de sua dissolução então
sobra soluto sem diluir no fundo do recipiente. Exemplo quando adoçamos exageradamente o nosso cafezinho que fica melado e sobra açúcar no fundo da xícara.
Soluções Gasosas
O ar da atmosfera que nos envolve é uma solução gasosa contendo vários gases diferentes. Gás nitrogênio (N2), gás oxigênio (O2), gás argônio (Ar), gás carbônico (CO2), gás ozônio (O3)
Soluções Líquidas
A água do mar é uma solução líquida contendo vários gases e vários sais dissolvidos na sua composição.
A água mineral engarrafada é uma solução muito diluída contendo vários gases e sais minerais dissolvidos na sua composição.
A água potável é uma solução.
A cerveja é uma solução.
Os refrigerantes gaseificados comerciais engarrafados são soluções.
O café coado que tomamos todos os dias é uma solução.
O soro fisiológico de uso hospitalar é uma solução.
O soro glicosado de uso hospitalar é uma solução.
O álcool etílico 42% é uma solução 42% etanol e 58% água.
Composição da Água Mineral Comercial
A água mineral pode variar a sua composição de fonte para fonte, portanto para se ter uma ideia dos compostos presentes em cada tipo de água, de-se ler o rótulo da embalagem que a contém o qual deverá apresentar seus valores. Por exemplo; uma água mineral poderá conter:
fluoreto de sódio 0,52 mg/litro
cloreto de sódio 11,62 mg/litro
bicarbonato de sódio 37,4 mg/litro
bicarbonato de potássio 6,40 mg/litro
sulfato de estrôncio 2,25 mg/litro
sulfato de cálcio 15,84 mg/litro.
bicarbonato de cálcio 102,72 mg/litro.
bicarbonato de magnésio 36,52 mg/litro.
óxido de zinco 0,01 mg/litro.
fluoreto de lítio 0,08 mg/litro
Para resolver as alternativas do exercício 1, basta multiplicar cada um dos valores por mil ou simplesmente deslocar a virgula três casas para a direita.
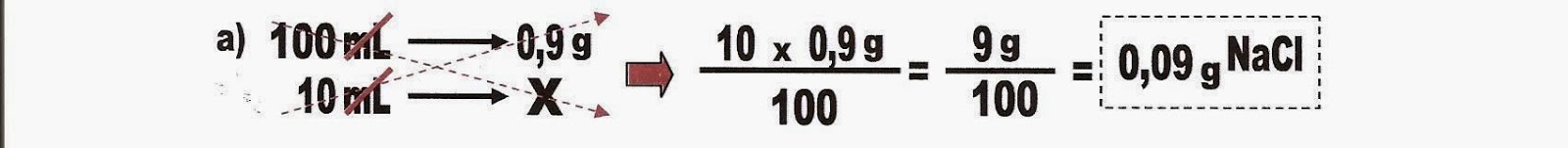

- A Densidade De Uma Solução
A Densidade de Uma Solução Definição A densidade de uma solução é dada pela massa em gramas do soluto presente nessa solução. É dada pela expressão: ...
- Concentração De Soluções
Concentração de Soluções 3ª aula 2ª Série A; B; C; D; TMA; TMB ...
- Lista De Exercícios Do Grupo De Estudo Do 3° Período
Bolsista: Nara Alinne Nobre da Silva...
- Avaliação De Química Nº 5 - Soluções
Avaliação de Química Geral 1) Calcule a concentração, em g/L e g/ml, de uma solução de nitrato de potássio, sabendo que ela possui 60g do sal em 300 cm3 de solução. 2) (Mackenzie-SP) Qual a concentração, em g/L da solução obtida ao se dissolverem...
- Avaliação De Química N° 3 - Soluções
Avaliação de Química Geral1) Calcule a concentração, em g/L e g/ml, de uma solução de nitrato de potássio, sabendo que ela possui 60g do sal em 300 cm3 de solução. 2) (Mackenzie-SP) Qual a concentração, em g/L da solução obtida ao se dissolverem...
Química
Soluções
Soluções
Soluções diluídas
A quantidade de soluto dissolvido é pequena. Exemplo os sais presentes na água mineral que tomamos.
Uma solução de hidróxido de sódio NaOH) 0,02 molar é uma solução diluída.
Uma solução de ácido clorídrico (0,01) molar é uma solução diluída.
Exemplos de Algumas Soluções
Solução de ácido bórico H3BO3.
Quando seco é um Cristal sólido pó incolor ou branco - o solvente é a água, 100 mL de água dissolve 5,14 g desse ácido.
Solução de bicromato de potássio K2Cr2O7 apresenta-se sólido, na forma de cristal - solvente água, dissolve-se 147 g dessa substância em água e completa-se para um litro. Para vários usos, determinação quantitativa de molibdênio, ou para lavagem de instrumentos que se exige certa assepsia, também é utilizado na determinação quantitativa de glicerina.
Soluções Concentradas
O soluto está dissolvido completamente até o seu limite de dissolução no solvente.
Uma solução de hidróxido de sódio (NaOH) 4 molar é uma solução concentrada.
Uma solução de ácido clorídrico (HCl) 4 molar é uma solução concentrada.
Soluções Saturadas
A quantidade do soluto presente na solução ultrapassou o limite de sua dissolução então
sobra soluto sem diluir no fundo do recipiente. Exemplo quando adoçamos exageradamente o nosso cafezinho que fica melado e sobra açúcar no fundo da xícara.
Soluções Gasosas
O ar da atmosfera que nos envolve é uma solução gasosa contendo vários gases diferentes. Gás nitrogênio (N2), gás oxigênio (O2), gás argônio (Ar), gás carbônico (CO2), gás ozônio (O3)
Soluções Líquidas
A água do mar é uma solução líquida contendo vários gases e vários sais dissolvidos na sua composição.
A água mineral engarrafada é uma solução muito diluída contendo vários gases e sais minerais dissolvidos na sua composição.
A água potável é uma solução.
A cerveja é uma solução.
Os refrigerantes gaseificados comerciais engarrafados são soluções.
O café coado que tomamos todos os dias é uma solução.
O soro fisiológico de uso hospitalar é uma solução.
O soro glicosado de uso hospitalar é uma solução.
O álcool etílico 42% é uma solução 42% etanol e 58% água.
Composição da Água Mineral Comercial
A água mineral pode variar a sua composição de fonte para fonte, portanto para se ter uma ideia dos compostos presentes em cada tipo de água, de-se ler o rótulo da embalagem que a contém o qual deverá apresentar seus valores. Por exemplo; uma água mineral poderá conter:
fluoreto de sódio 0,52 mg/litro
cloreto de sódio 11,62 mg/litro
bicarbonato de sódio 37,4 mg/litro
bicarbonato de potássio 6,40 mg/litro
sulfato de estrôncio 2,25 mg/litro
sulfato de cálcio 15,84 mg/litro.
bicarbonato de cálcio 102,72 mg/litro.
bicarbonato de magnésio 36,52 mg/litro.
óxido de zinco 0,01 mg/litro.
fluoreto de lítio 0,08 mg/litro
Soluções Sólidas
Liga metálica de cobre (Cu) e níquel (Ni) é uma solução
O elemento químico níquel tem densidade de 8,9 g/Cm3, ponto de fusão de 1455oC e ponto de ebulição 2913 oC. O cobre tem o ponto de fusão 1084OC, ponto de ebulição 2567OC e densidade de 8,92 g/cm3.O níquel é muito solúvel no cobre por isso facilmente pode ser transformado em liga. A Liga metálica de cobre (Cu) e níquel (Ni) se apresenta em diversas porcentagens de acordo com a necessidade de resistência da peça a ser produzida, por exemplo; fabrica-se a liga com 95 % de cobre e 5% de níquel, com 90 % cobre 10 % níquel, ou a liga de 70% de cobre e 30% níquel. Todas essas ligas possuem também um pouco de ferro e manganês. Essas ligas; precisamente a com 5% de níquel é utilizada na fabricação de motores de veículos marítimos pois é resistente a corrosão pela umidade, sal marinho e também a ácidos. Outra liga pode atingir 65% de níquel e 34 % cobre com um pouco de ferro e manganês incluso nessa solução, outras ligas 55 % de níquel e 44% de cobre, com ferro e manganês. A liga com 20 % de níquel 80 % cobre tem sua aplicação na fabricação de lâminas de turbinas, chapas e tiras, resistores elétricos , recipientes de transistores, guias de ondas de radar, aquecedores de água doméstico, moedas e medalhas cunhadas. A mistura 95 % cobre e 5% níquel é utilizado na fabricação de chapas placas e tubos que são destinadas para tubos condutores de água salgada e também em anéis de mangueiras de Bombeiros.
Exercícios
Preparo de soluções
1) Transformar os seguintes valores de litro para mililitros
Preparo de soluções
1) Transformar os seguintes valores de litro para mililitros
a) | 0,01 L | 10 mL | j) | 0,91 L | 910 mL |
b) | 0,018 L | k) | 1,05 L | ||
c) | 0,02 L | l) | 1,15 L | ||
d) | 0,025 L | m) | 1,19 L | ||
e) | 0,093 L | n) | 1,25 L | ||
f) | 0,155 L | O) | 1,51 L | ||
g) | 0,200 L | p) | 2,09 L | ||
h) | 0,23 L | q) | 2,26 L | ||
i) | 0,551 L | r) | 2,451 L | ||
j) | 0,75 L | s) | 2,55 L |
Para resolver as alternativas do exercício 1, basta multiplicar cada um dos valores por mil ou simplesmente deslocar a virgula três casas para a direita.
2) Quanto do soluto de cloreto de sódio (NaCl) em grama (s) devo pesar numa balança analítica para preparar os seguintes volumes de solução fisiológica 0,9%.
a) | 0,01 L | 10 mL | j) | 0,9 L |
b) | 0,02 L | k) | 1,0 L | |
c) | 0,03 L | l) | 1,01 L | |
d) | 0,05 L | m) | 1,1 L | |
e) | 0,09 L | n) | 1,25 L | |
f) | 0,1 L | O) | 1,5 L | |
g) | 0,2 L | p) | 2,0 L | |
h) | 0,3 L | q) | 2,06 L | |
i) | 0,5 L | r) | 2,25 L | |
j) | 0,75L | s) | 2,55 L |
Resolução das alternativas
Sugiro Primeiramente transformar os valores de litro para mililitros.
Pode-se resolver as questões com uma simples regra de três. Você ainda pode simplesmente multiplicar todos os volumes por 0,9 e dividir todos os resultados por 100.
Resolvendo a alternativa a.
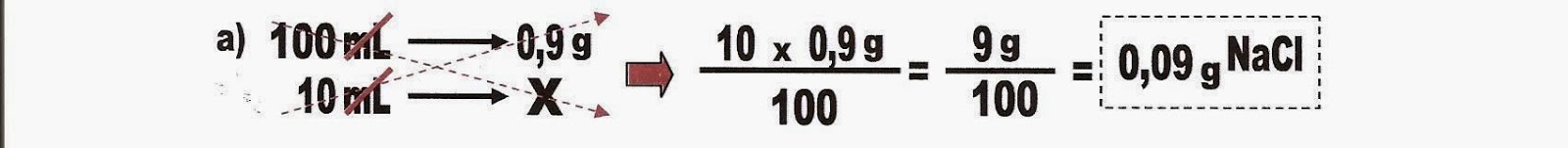
3) Número de partículas contaminantes na solução.
O chumbo pode contaminar a água potável poluindo suas fontes através de aditivos da gasolina tintas etc. Causa náuseas, irritabilidade e danos ao cérebro. A concentração máxima permitida de chumbo na água potável para que não cause efeitos tóxicos sobre a saúde humana é de 0,01 mg/L. Foram separadas diversas quantidades dessa água conforme demonstrado abaixo. Pergunta-se qual o número de partículas de chumbo presentes para cada volume? Dados massa do chumbo 207.
a) | 0,01 L | 10 mL | j) | 0,9 L = 900 mL | |
b) | 0,02 L | k) | 1,0 L | ||
c) | 0,03 L | l) | 1,01 L | ||
d) | 0,05 L | m) | 1,1 L | ||
e) | 0,09 L | n) | 1,25 L | ||
f) | 0,1 L | O) | 1,5 L | ||
g) | 0,2 L | p) | 2,0 L | ||
h) | 0,3 L | q) | 2,06 L | ||
i) | 0,5 L | r) | 2,25 L | ||
j) | 0,75L | s) | 2,55 L |
Resolução das alternativas da questão número 3.
Primeiramente achar quantas partículas de chumbo há em 0,01 mg por litro.

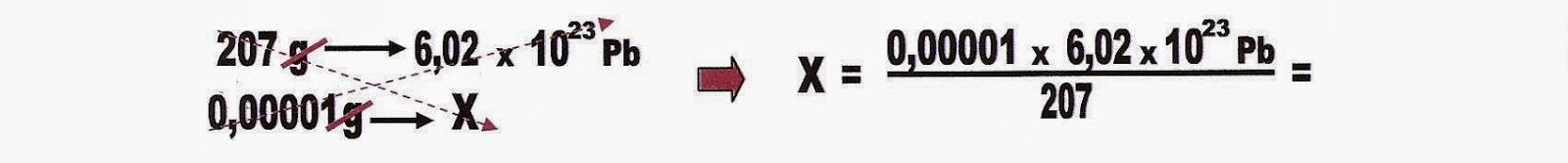
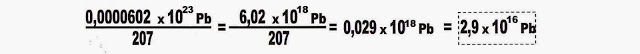
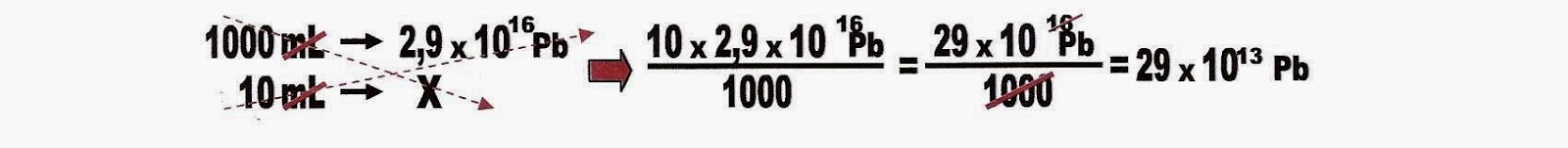 Em 10 mililitros de água há 290 000 000 000 000 duzentos e noventa trilhões de partículas de chumbo.
Em 10 mililitros de água há 290 000 000 000 000 duzentos e noventa trilhões de partículas de chumbo.
Continue resolvendo o restante das alternativas da questão número 3.
4) Para preparar as seguintes soluções relacionadas abaixo de soro glicosado a 5%, quanto de glicose C6H12O6deve ser adicionado para cada volume?
Primeiramente achar quantas partículas de chumbo há em 0,01 mg por litro.
Podemos usar a regra de três.

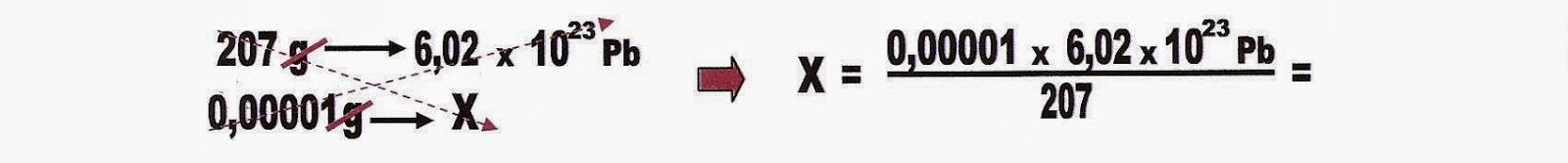
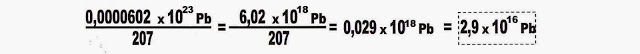
Sabemos que há 29 000 000 000 000 000 (vinte e nove quatrilhões) de partículas de chumbo em um litro de água cuja concentração é de 0,01 mg.
Resolvendo a alternativa a, da questão número 3.
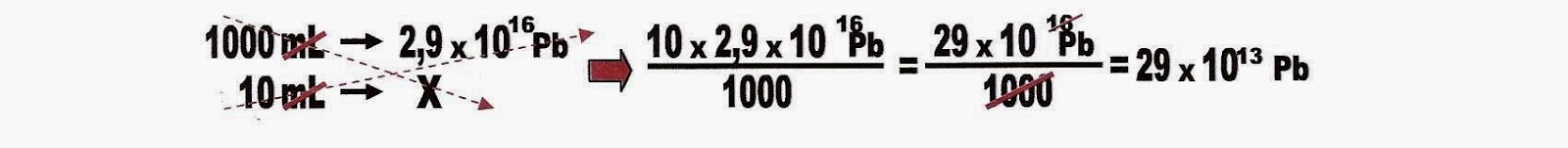
Continue resolvendo o restante das alternativas da questão número 3.
4) Para preparar as seguintes soluções relacionadas abaixo de soro glicosado a 5%, quanto de glicose C6H12O6deve ser adicionado para cada volume?
a) | 0,01 L | 10 mL | j) | 0,9 L | 900 mL |
b) | 0,02 L | k) | 1,0 L | ||
c) | 0,03 L | l) | 1,01 L | ||
d) | 0,05 L | m) | 1,1 L | ||
e) | 0,09 L | n) | 1,25 L | ||
f) | 0,1 L | O) | 1,5 L | ||
g) | 0,2 L | p) | 2,0 L | ||
h) | 0,3 L | q) | 2,06 L | ||
i) | 0,5 L | r) | 2,25 L | ||
j) | 0,75L | s) | 2,55 L |
Resolução da alternativa a.
Primeiramente transformar os volumes de litro para mililitro.
Na sequência utilize a regra de três.

5) Considerando que cada litro de água do mar contém aproximadamente 2,95 gramas de sal cloreto de sódio (NaCl). Qual o volume dessa água eu terei que evaporar para obter uma tonelada desse sal cristalizado? Assinale a alternativa correta.
Primeiramente transformar os volumes de litro para mililitro.
Na sequência utilize a regra de três.

Resolva o restante das alternativas do exercício 4.
a) 3 . 104 t b) 3,39 . 102 t c) 1,5 . 105 t d) 5,5 .103 t e) 10,1 . 104 t

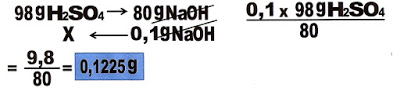
8) Deseja-se saber o pH de uma solução em que foi juntado 200 mL de NaOH 0,2 molar, com 200 mL de H2SO4 0,2 molar. Se ao juntar as duas partes a solução não foi neutralizada totalmente, qual é a molaridade da solução final.

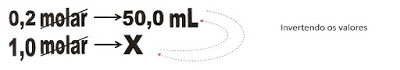
6) Sabendo que 1 molar de ácido clorídrico neutraliza 1 molar de hidróxido de sódio, numa titulação ácido-base, foi colocado num erlenmayer 50.0 mL de hidróxido de sódio de concentração 0,2 molar. Quanto mL de ácido clorídrico 1,0 molar, você deverá titular sobre a solução de soda caustica do erlenmeyer para neutraliza-lo?
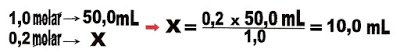
7) 250 mL de hidróxido de sódio (NaOH) 0,01 molar precisa ser neutralizado pelo ácido sulfúrico (H2SO4). Pergunta-se: quantas gramas desse ácido serão necessárias para a neutralização total da base?
Resolução.


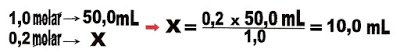
7) 250 mL de hidróxido de sódio (NaOH) 0,01 molar precisa ser neutralizado pelo ácido sulfúrico (H2SO4). Pergunta-se: quantas gramas desse ácido serão necessárias para a neutralização total da base?
Resolução.


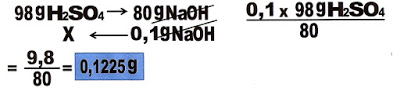
8) Deseja-se saber o pH de uma solução em que foi juntado 200 mL de NaOH 0,2 molar, com 200 mL de H2SO4 0,2 molar. Se ao juntar as duas partes a solução não foi neutralizada totalmente, qual é a molaridade da solução final.
A reação pode ser representada pela equação:


Ou ainda pelo esquema:
Achar a massa gasta do hidróxido de sódio (NaOH) em 1 litro de solução.

Achar a massa do ácido sulfúrico (H2SO4) em 1 litro de solução.

Achar a massa do hidróxido de sódio em 200 mL de solução.

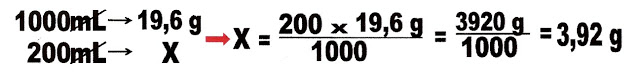
Sobra do ácido que não reagiu com o hidróxido de sódio. A solução é ácida.
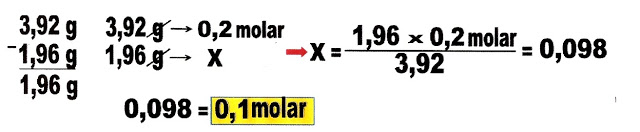
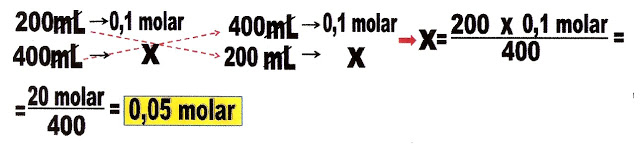
Como duplicou o volume da solução, que de 200 mL foi para 400 mL, a molaridade final: será
9) ( Fuvest ? SP) Um analgésico em gotas deve ser ministrado na quantidade de 3,0 mg por quilograma de peso corporal, não podendo contudo exceder 200 mg por dose. Cada gota contém 5,0 mg de analgésico. Quantas gotas deverão ser administradas a um paciente de 80,0 kg? Indique seu raciocínio.
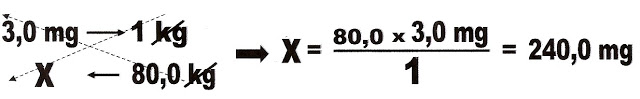
Observe que o indivíduo não pode tomar mais que 200.0 mg do analgésico
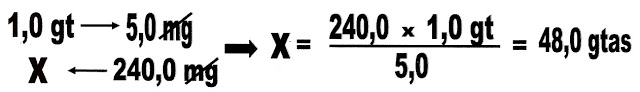
Se necessita tomar 200 mg do medicamento, quantas gotas o indivíduo terá que tomar?
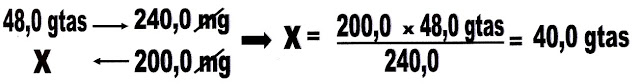
10) Foi aplicado no Enem e na UFRJ. No cultivo hidropônico de hortaliças, as plantas não são cultivadas diretamente no solo. Uma solução contendo nutrientes circula entre as raízes. A tabela a seguir apresenta a composição recomendada de alguns nutrientes para o cultivo hidropônico do alface.
No cultivo hidropônico de hortaliças, as plantas não são cultivadas diretamente no solo. Uma solução contendo nutrientes circula entre as raízes. A tabela a seguir apresenta a composição recomendada de alguns nutrientes para o cultivo hidropônico do alface.
Tabela
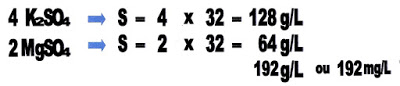
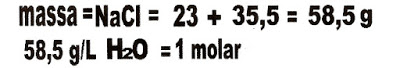
Calculando a molaridade da solução.



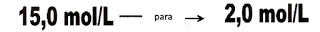
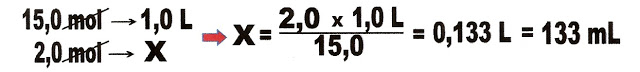
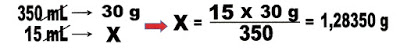
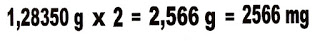
Achar a massa gasta do hidróxido de sódio (NaOH) em 1 litro de solução.

Achar a massa do ácido sulfúrico (H2SO4) em 1 litro de solução.

Achar a massa do hidróxido de sódio em 200 mL de solução.

Achar a massa do ácido sulfúrico em 200 mL de solução.
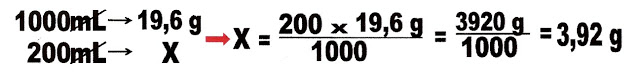
Sobra do ácido que não reagiu com o hidróxido de sódio. A solução é ácida.

Como duplicou o volume da solução, que de 200 mL foi para 400 mL, a molaridade final: será

9) ( Fuvest ? SP) Um analgésico em gotas deve ser ministrado na quantidade de 3,0 mg por quilograma de peso corporal, não podendo contudo exceder 200 mg por dose. Cada gota contém 5,0 mg de analgésico. Quantas gotas deverão ser administradas a um paciente de 80,0 kg? Indique seu raciocínio.
Resolução do problema utilizando regra de três.
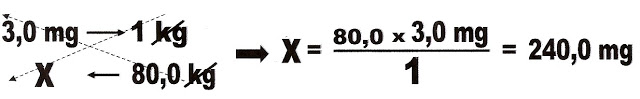
Observe que o indivíduo não pode tomar mais que 200.0 mg do analgésico
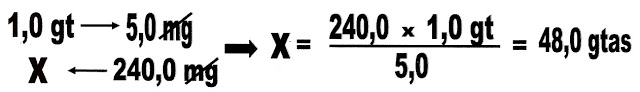
Se necessita tomar 200 mg do medicamento, quantas gotas o indivíduo terá que tomar?
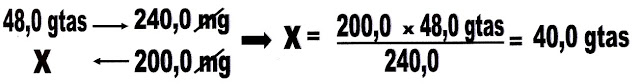
10) Foi aplicado no Enem e na UFRJ. No cultivo hidropônico de hortaliças, as plantas não são cultivadas diretamente no solo. Uma solução contendo nutrientes circula entre as raízes. A tabela a seguir apresenta a composição recomendada de alguns nutrientes para o cultivo hidropônico do alface.
No cultivo hidropônico de hortaliças, as plantas não são cultivadas diretamente no solo. Uma solução contendo nutrientes circula entre as raízes. A tabela a seguir apresenta a composição recomendada de alguns nutrientes para o cultivo hidropônico do alface.
Tabela
Nutrientes | Concentração mg/L |
K - potássio | 312 |
Mg - Magnésio | 48 |
S - enxofre | ? |
Foram utilizados sulfato de potássio (K2SO4) e o sulfato de magnésio (MgSO4) para preparar uma solução nutriente de acordo com as concentrações apresentadas na tabela.
Não tendo a concentração de enxofre, na tabela, pergunta-se: a concentração em mg/L de enxofre nesta solução será igual a.
Dados a massas molares:
Mg = 24 g/mol
K = 39 g/mol
S = 32 g/mol
Para achar a massa do enxofre gasta para preparar a solução, basta somar os 4 enxofres do composto sulfato de potássio, mais os dois enxofres do composto sulfato de magnésio = 6 x 32 = 192 g. Como a concentração no problema foi dado em miligrama por litro, basta passar automaticamente a massa de grama para miligrama.
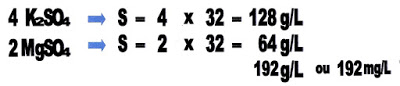
a) 32 mg/L
b) 64 mg/L
c) 128 mg/L
d) 192 mg/L
e) 224 mg/L
11) O sal de cozinha, cloreto de sódio (NaCl) a 25 ºC e 1 atm, 36,0 gramas dissolve totalmente em 100 mL de água. Pede-se calcular a molaridade dessa solução.
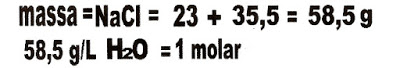
Calculando a molaridade da solução.

Quanto de água você deve acrescentar na solução para transforma-la em solução 1 molar?


12) Para uso de rotina num laboratório, deseja-se preparar 1 litro de solução de H2SO4, 2 molar a partir do ácido concentrado 15 mol/L. Qual alíquota do ácido concentrado devo usar na preparação da solução?
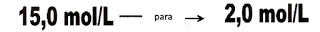
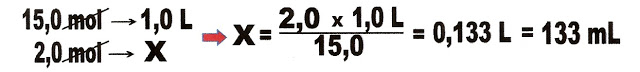
Devo medir 133 mL da solução concentrada de H2SO4, para preparar 1 litro de solução 2 molar.
13) Um frasco de leite de magnésia contém 350 mL da solução, que contém 30 gramas do composto ativo Mg(OH)2. Ao tomar 2 colheres de sopa de 15 mL cada uma, quantas miligramas do composto o indivíduo em tratamento tomou?
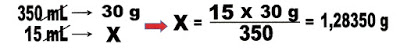
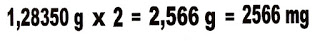
loading...
- A Densidade De Uma Solução
A Densidade de Uma Solução Definição A densidade de uma solução é dada pela massa em gramas do soluto presente nessa solução. É dada pela expressão: ...
- Concentração De Soluções
Concentração de Soluções 3ª aula 2ª Série A; B; C; D; TMA; TMB ...
- Lista De Exercícios Do Grupo De Estudo Do 3° Período
Bolsista: Nara Alinne Nobre da Silva...
- Avaliação De Química Nº 5 - Soluções
Avaliação de Química Geral 1) Calcule a concentração, em g/L e g/ml, de uma solução de nitrato de potássio, sabendo que ela possui 60g do sal em 300 cm3 de solução. 2) (Mackenzie-SP) Qual a concentração, em g/L da solução obtida ao se dissolverem...
- Avaliação De Química N° 3 - Soluções
Avaliação de Química Geral1) Calcule a concentração, em g/L e g/ml, de uma solução de nitrato de potássio, sabendo que ela possui 60g do sal em 300 cm3 de solução. 2) (Mackenzie-SP) Qual a concentração, em g/L da solução obtida ao se dissolverem...
