Química
Bolsista: Roniel Francisco
Notícia:
- Ciclo Do Carbono
Bolsista: Luzia Morais Dos Santos O carbono é um elemento químico fundamental para a estrutura dos seres vivos. Seu número atômico é 6 e sua massa 12,01 u.m.a. O carbono participa da composição química...
- Quem Vence? Um PaÍs Ou Uma Empresa?
Bolsista: Alessandro R. Barbosa Oi seguidores e amigos do QUIPIBID! Hoje atualizamos nossa coluna de atualidades com uma reportagem do portal G1, sobre reportagem de jornal que diz que...
- Isótopos, Isóbaros E Isótonos
Bolsista: Litton Jr.Olá amigos do QUIPIBID! Essa semana na nossa coluna de dicas de vestibular iremos falar sobre os isótonos, isóbaros e isótonos, o conteúdo é curto e de facil compreensão, mas para isso é necessário entender algumas características...
- Avaliação De Química Nº 2 - Isótopos - Isóbaros E Isótonos
1) São dados três átomos genéricos A, B e C. O átomo A tem número atômico 78 e número de massa 174. O átomo C tem 98 nêutrons, sendo isótopo de A. O átomo B é isóbaro de C e isótono de A. O número de elétrons do átomo B é: 2) São...
- Avaliação N° 1 - Estrutura Atômica
QUESTÕES: 1) Descubra o número de atômico e o número de massa do átomo de cloro, sabendo que ele tem dezessete prótons e dezoito nêutrons.a) número atômico 17 e massa 30b) número atômico 18 e massa 35c) número atômico 17 e massa 35d) número...
Química
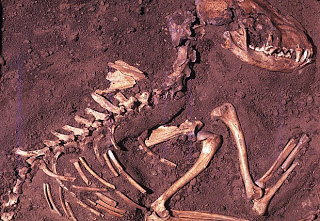
COMO SE DETERMINA A IDADE DE UM FÓSSIL
Bolsista: Roniel Francisco
Olá pessoal do QUIPIBID, nessa semana, na coluna de atualidades, vamos falar um pouco sobre uma matéria do portal G1, exibida dia 15/11/13, que relata o surgimento do cachorro doméstico na Europa, há pelo menos 19 mil anos atrás. Mas como identificar aproximadamente a idade dos fósseis encontrados?

Notícia:
Uma análise detalhada de DNA apontou que os cães modernos surgiram na Europa entre 19 mil e 32 mil anos atrás.
Pesquisas anteriores haviam sugerido, no entanto, que a origem do melhor amigo do homem seria o leste asiático ou o oriente médio. O debate sobre qual teoria é verdadeira, não deve terminar tão cedo. Todos concordam, porém, que os cães se originaram dos lobos.
Durante um longo processo, os cães foram domesticados e se mostraram úteis para caçar e proteger seus donos.
O DNA dos cães modernos mostrou grandes semelhanças com as espécimes de antigos cachorros europeus e também com o dos lobos europeus modernos.
Um dos responsáveis pelo estudo disse que agora há três possíveis hipóteses sobre as origens dos cães e que o tipo de lobo que deu origem a esses animais domésticos já foi extinto. (fonte:Notícia)
Entendendo como se determina a idade de um fóssil
Primeiramente vamos esclarecer o que são isótopos. Duas espécies dizem-se isótopos quando apresentam mesmo número atômico e diferem no número de massa, ou seja, apresentam maior ou menor número de nêutrons.
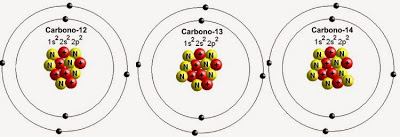
No caso do carbono existem inúmeros isótopos, sendo que os mais famosos vão do 8 até 22. Os isótopos mais abundantes e mais importantes são o 11, 12, 13 e 14 (ver figura abaixo). O fato de serem os isótopos mais importantes deve-se ao fato dos seus tempos de meia-vida serem grandes, no caso do 11 o tempo de meia-vida é de aproximadamente 20 minutos e o 14 cerca de 5700 anos.
ALGUNS ISÓTOPOS DO CARBONO 12

O carbono-12, por ser um isótopo estável, não é radioativo e por ser o mais abundante está envolvido em toda a química orgânica. Já o isótopo de carbono-14 é usado na datação radioativa, em que é possível determinar a idade de certos compostos orgânicos e inorgânicos através da medição da atividade deste isótopo. No carbono-14 a meia-vida ou período de semidesintegração é de 5700 anos, ou seja, este é o tempo necessário para uma determinada massa deste isótopo instável decair para a metade da sua massa. Logo, se tivéssemos 10 g de carbono-14, daqui a 5700 anos teríamos 5 g desse mesmo elemento.
Datação radioativa
O método usado para determinar a idade de um fóssil é chamado de datação radioativa, se baseia no fenômeno da radioatividade, descoberto no final do século XIX. A radioatividade faz os átomos perderem partículas (prótons ou nêutrons) na forma de radiação, causando variação no seu número de massa ou em seu número atômico. No caso de fósseis de seres vivos, costuma-se usar carbono 14 (com seis prótons e oito nêutrons) para fazer a datação. O carbono 14 emite radiação, perdendo dois nêutrons e se transformando em carbono 12. Em 5.700 anos, certa quantidade de carbono 14 ficará reduzida à metade, sendo a outra metade transformada em carbono-12. Por isso, esse tempo é chamado de meia-vida.
A química está presente nesse processo, mais precisamente o elemento carbono. A datação de um fóssil pode ser feita com base no percentual já conhecido do carbono-14 em relação ao carbono-12 da matéria viva.
O carbono-14 é formado continuamente na atmosfera e é resultante do processo de bombardeio de raios cósmicos. Ele entra no processo de fotossíntese e em consequência disso todos os seres vivos possuem em sua composição geral certa porcentagem de carbono-14, ainda que em pequena quantidade.
Quando o ser vivo morre inicia-se uma diminuição da quantidade de carbono-14, devido a sua desintegração radioativa. Os cientistas então, se baseiam no cálculo comparativo entre a quantidade habitual encontrada na matéria viva, e aquela que foi descoberta no fóssil, determinando assim a idade do mesmo.
Espero que tenham gostado, bons estudos e até a próxima.
Referências:
http://g1.globo.com/ciencia-e-saude/noticia/2013/11/caes-modernos-surgiram-na-europa-ha-pelo-menos-19-mil-anos-diz-estudo.html
www.mundoeducacao.com/quimica/datacao-fosseis.htm
http://mundoestranho.abril.com.br/materia/como-edeterminada-a-idade-de-um-fossil
loading...
- Ciclo Do Carbono
Bolsista: Luzia Morais Dos Santos O carbono é um elemento químico fundamental para a estrutura dos seres vivos. Seu número atômico é 6 e sua massa 12,01 u.m.a. O carbono participa da composição química...
- Quem Vence? Um PaÍs Ou Uma Empresa?
Bolsista: Alessandro R. Barbosa Oi seguidores e amigos do QUIPIBID! Hoje atualizamos nossa coluna de atualidades com uma reportagem do portal G1, sobre reportagem de jornal que diz que...
- Isótopos, Isóbaros E Isótonos
Bolsista: Litton Jr.Olá amigos do QUIPIBID! Essa semana na nossa coluna de dicas de vestibular iremos falar sobre os isótonos, isóbaros e isótonos, o conteúdo é curto e de facil compreensão, mas para isso é necessário entender algumas características...
- Avaliação De Química Nº 2 - Isótopos - Isóbaros E Isótonos
1) São dados três átomos genéricos A, B e C. O átomo A tem número atômico 78 e número de massa 174. O átomo C tem 98 nêutrons, sendo isótopo de A. O átomo B é isóbaro de C e isótono de A. O número de elétrons do átomo B é: 2) São...
- Avaliação N° 1 - Estrutura Atômica
QUESTÕES: 1) Descubra o número de atômico e o número de massa do átomo de cloro, sabendo que ele tem dezessete prótons e dezoito nêutrons.a) número atômico 17 e massa 30b) número atômico 18 e massa 35c) número atômico 17 e massa 35d) número...
