Química
- Molaridade
Molaridade Definição Molaridade é a concentração do mol de uma substância que é a sua massa em gramas em um litro de solução. O que...
- Cálculos Das Massas Átomos, Moléculas E Compostos Iônicos
Cálculos das Massas ...
- Avogadro E A Teoria AtÔmico-molecular
Bolsista: Walmira Gomes Olá pessoal do Quipibid, estamos de volta com as nossas colunas, atualizadas e com novidades!Vamos falar sobre as contribuições de Avogadro para a Teoria atômico-molecular e para a evolução da química.Amedeo di Quarema Avogadro...
- Avogadro - A Sua ContribuiÇÃo Para A QuÍmica
Bolsista: Leidiane R. Rosa Químico e físico italiano, Amedeo Avogadro, nasceu em Turim, em 9 de agosto de 1776, e faleceu em 9 de julho de 1856. Foi Conde de Quarequa e de Cerreto herdou o título de nobreza do pai, também foi presidente...
- Avaliação N° 1 - Estrutura Atômica
QUESTÕES: 1) Descubra o número de atômico e o número de massa do átomo de cloro, sabendo que ele tem dezessete prótons e dezoito nêutrons.a) número atômico 17 e massa 30b) número atômico 18 e massa 35c) número atômico 17 e massa 35d) número...
Química
Número de Partículas
Número de Partículas
Constante de Avogadro
Foi Amadeu Avogadro, Italiano que em 1811 propôs pela primeira vez um valor numérico constante que em determinada pressão e temperatura, coincidiria com o número de moléculas ou de partículas de qualquer tipo de gás.
Em 1909 o francês Jean Perrin com seus trabalhos, utilizando diversos métodos na determinação do valor da Constante das massas, se propôs a nomear com o nome de Constante de Avogadro, que coincidiria com o número de 1 mol de gás oxigênio que pesaria 32 gramas.
Exemplo:
A massa do gás hidrogênio (H2) é 2 u.



Exercícios
Constante de Avogadro
Foi Amadeu Avogadro, Italiano que em 1811 propôs pela primeira vez um valor numérico constante que em determinada pressão e temperatura, coincidiria com o número de moléculas ou de partículas de qualquer tipo de gás.
Em 1909 o francês Jean Perrin com seus trabalhos, utilizando diversos métodos na determinação do valor da Constante das massas, se propôs a nomear com o nome de Constante de Avogadro, que coincidiria com o número de 1 mol de gás oxigênio que pesaria 32 gramas.
Mol seria a massa em gramas de qualquer substância a nível atômico ou molecular. O mol corresponde ao número de Avogadro que corresponde a 6.02 x 1023partículas.
Exemplo:
A massa do gás hidrogênio (H2) é 2 u.
Em mol a substância gás hidrogênio (H2), possui 6,02 x 1023 partículas ou moléculas desse gás que corresponde a 2 gramas.
Então 6,02 x 1023 partículas = 2,0 g de H2 = 1 mol.
Observe o número de partículas de algumas substâncias.
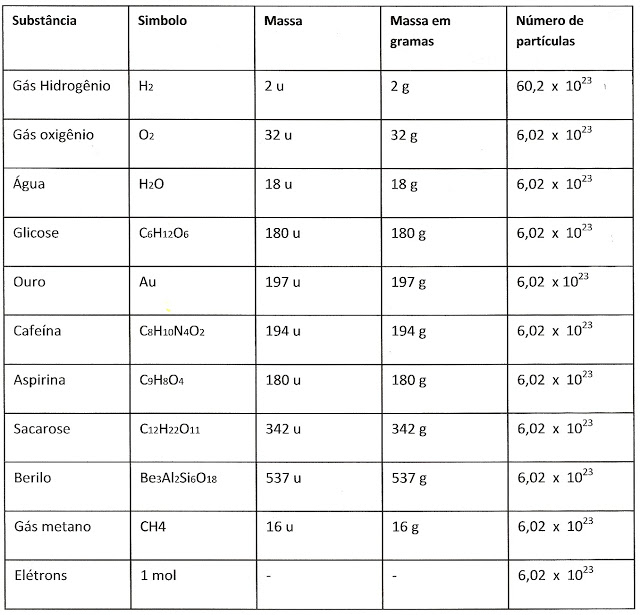
Vejamos outro exemplo mais explicito.
Observe o número de partículas de algumas substâncias.

Vejamos outro exemplo mais explicito.
1) Calcular o número de partículas de NaCl que há nas seguintes massas dessa substância.
 2) Qual é o número de partículas ou moléculas de água em um copo com 100 mL ou 100 g de água? |



Exercícios
3) Conhecendo o número de mol de uma substância, podemos calcular o número de partículas que certa quantidade dessa substância possui. Por exemplo, a aspirina, ou seja; o ácido-2-acetoxibenzoico (C9H8O4), tem o peso molecular de 180 g/mol.
Esse medicamento é analgésico, antipirético e anti inflamatório, geralmente é comercializado em comprimidos de 100 mg, 250 mg, 500 mg, 1000 mg.
Conforme a posologia do bulário, o médico indicou 1 comprimido de 500 mg de ácido acetil salicílico, 3 vezes ao dia, a um paciente. Pergunta-se, quantas moléculas do ácido acetilsalicílico esse indivíduo ingeriu diariamente?

4) (Enem ? 2013) (adaptado) afirma-se cientificamente que 40 g/mol de cálcio, coincide com o número de Avogadro, ou com o valor de 6 x 1023 átomos desse elemento químico. Pede-se para calcular o número de átomos que o indivíduo deverá ingerir para suprir suas necessidades diárias.
É de nosso interesse esse conhecimento, pois as pesquisas afirmam, que o brasileiro ingere somente 500 mg de cálcio diariamente, sendo necessário, o dobro dessa quantidade. Conforme dados clínicos, essa ingestão evita a osteoporose, doença dos ossos, que causa a diminuição da massa óssea corporal, além de torná-los enfraquecidos e quebradiços.
Dadas as alternativas abaixo, assinale somente a correta.
Dadas as alternativas abaixo, assinale somente a correta.
a) 7,5 × 1021 b) 1,5 × 1022 c) 7,5 × 1023 d) 1,5 × 1025 e) 4,8 × 1025
Resolução



O dobro coincide com:

loading...
- Molaridade
Molaridade Definição Molaridade é a concentração do mol de uma substância que é a sua massa em gramas em um litro de solução. O que...
- Cálculos Das Massas Átomos, Moléculas E Compostos Iônicos
Cálculos das Massas ...
- Avogadro E A Teoria AtÔmico-molecular
Bolsista: Walmira Gomes Olá pessoal do Quipibid, estamos de volta com as nossas colunas, atualizadas e com novidades!Vamos falar sobre as contribuições de Avogadro para a Teoria atômico-molecular e para a evolução da química.Amedeo di Quarema Avogadro...
- Avogadro - A Sua ContribuiÇÃo Para A QuÍmica
Bolsista: Leidiane R. Rosa Químico e físico italiano, Amedeo Avogadro, nasceu em Turim, em 9 de agosto de 1776, e faleceu em 9 de julho de 1856. Foi Conde de Quarequa e de Cerreto herdou o título de nobreza do pai, também foi presidente...
- Avaliação N° 1 - Estrutura Atômica
QUESTÕES: 1) Descubra o número de atômico e o número de massa do átomo de cloro, sabendo que ele tem dezessete prótons e dezoito nêutrons.a) número atômico 17 e massa 30b) número atômico 18 e massa 35c) número atômico 17 e massa 35d) número...
