Química
Álcoois
Álcoois são compostos orgânicos contendo uma ou mais hidroxilas (OH) que lhe confere a característica própria da substância, estão ligadas diretamente a átomo (s) de carbono (s) saturado (s). Os álcoois têm cheiro característico, geralmente são solúveis em água e formam um grupo extenso de tipos diferentes. São líquidos incolores, no entanto; os de cadeias carbônicas com o número superior a doze carbonos são sólidos.
- Funções Orgânicas E Nomeclatura
Dentro da química orgânica existem as funções orgânicas (compostos ôrganicos de características químicas e físicas semelhantes). Existem muitas funções, sendo as mais comuns:· Hidrocarbonetos (Alcanos, Alcenos, Alcinos, Alcadienos, Alcadiinos,...
- O Álcool Do Nosso Dia A Dia
Tatiane dos Santos Olá amigos do blog! O assunto de hoje é bastante conhecido por todos, o álcool ou quimicamente falando etanol, ou melhor, álcool etílico!O etanol é um composto orgânico obtido na maioria das vezes da cana de açúcar, porém...
- ?as Bebidas Fortes Fazem Os Homens Fracos?
Bolsista: Alessandro R. Barbosa Oi seguidores e amigos do QUIPIBID! Hoje atualizamos nossa coluna de atualidades com uma reportagem do portal G1, sobre a Europa ser a região líder no...
- Oxidação Do álcool Com Dicromato De Potássio.
OXIDAÇÕES DE ÁLCOOIS COM DICROMATO DE POTÁSSIO Fácil e ilustrativo Embora façamos muita menção por aqui ao emprego do dicromato de potássio (K2Cr2O7) como agente oxidante em reações inorgânicas (que é a base do método de titulação...
- Propriedades Químicas Dos Alcoóis
Os compostos pertencentes a esta função química são muito reativos, devido a presença da hidroxila ou oxidrila. O hidrogênio confere um leve caráter ácido ao grupo oxidrila, sendo, portanto mais reativos que os hidrocarbonetos, devido a polaridade...
Química
Química Orgânica - Álcoois
Há álcoois que possuem anel benzênico na sua estrutura molecular, nesse caso a hidroxila não se liga diretamente ao carbono do anel benzênico, mas deverá estar ligado a outro carbono saturado que se liga ao anel.
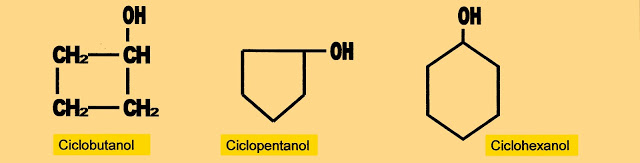
Os álcoois com anel cíclico, possuem uma cadeia cíclica na sua estrutura molecular, que no entanto não é a cadeia carbônica do benzeno, nesses; a hidroxila se liga ao carbono saturado do anel sem a necessidade de um carbono intermediário.
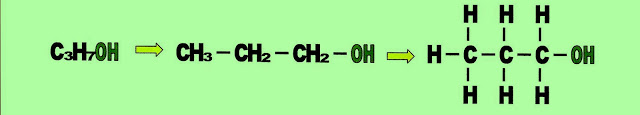 Butanol
Butanol
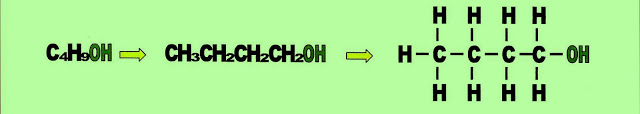 Pentanol
Pentanol
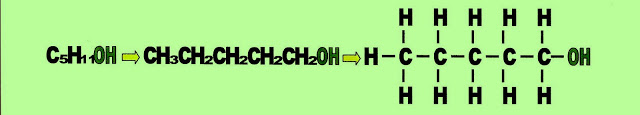
Álcool Cíclico ciclo-hexanol
No álcool ciclo-hexanol, a hidroxila está ligada diretamente ao carbono insaturado do anel.
 Ciclo hexanol ciclo hexanol
Ciclo hexanol ciclo hexanol






 Etanol
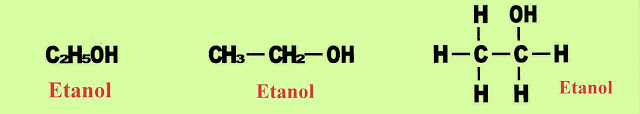
Etanol
Etanol - tem 2 carbonos ?et? + ?an? + a terminação ?ol?.
Propanol
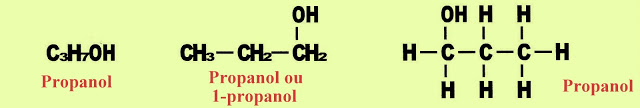
Propanol - tem 3 carbonos na cadeia ?prop? + ?an? + a terminação ?ol?.
Butanol
Butanol - tem 4 carbonos na cadeia ?but? + ?an? + a terminação ?ol?.
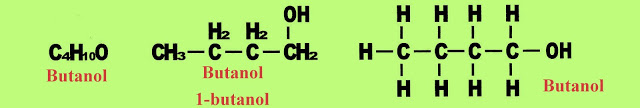
Pentanol - tem 5 carbonos na cadeia ?pent? + ?an? + a terminação ?ol?.
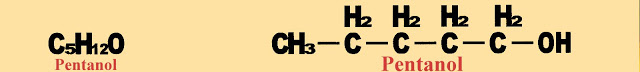
Hexanol ou 1 hexanol
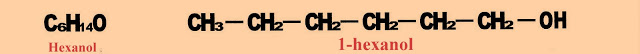
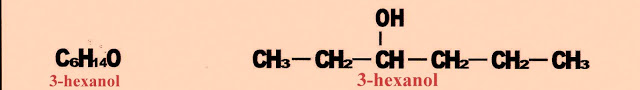



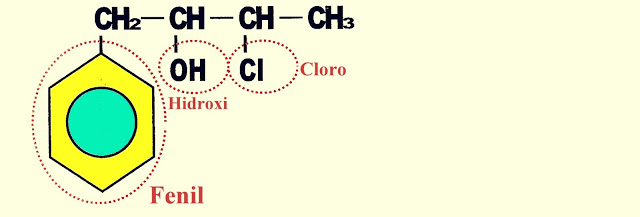
1-fenil-2-hidroxi-3-cloro-butanol - a hidroxila se torna uma ramificação que leva o nome de hidroxi.

Nomenclatura de Álcoois de Cadeias Carbônicas Insaturadas
Estes álcoois apresentam suas cadeias carbônicas como duplas ou triplas ligações entre seus carbonos.
2-metil-2-buten-1-ol (IUPAC)




Nome oficial: 2-metil-2-propanol
Nome usual: álcool terci-butílico
Nome segundo Kolbe: trimetil-carbinol.







Os álcoois com anel cíclico, possuem uma cadeia cíclica na sua estrutura molecular, que no entanto não é a cadeia carbônica do benzeno, nesses; a hidroxila se liga ao carbono saturado do anel sem a necessidade de um carbono intermediário.
Exemplos de Alguns Álcoois Mais Comuns
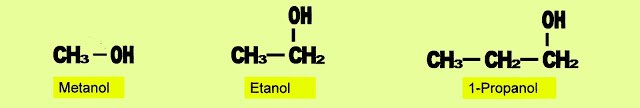
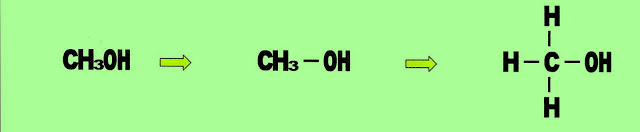
Metanol
 Propanol
Propanol
Metanol

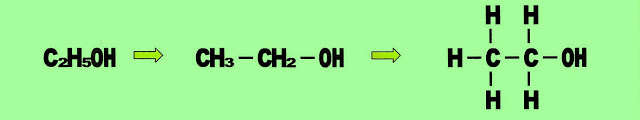
Etanol




No álcool ciclo-hexanol, a hidroxila está ligada diretamente ao carbono insaturado do anel.

Fenol Não é Álcool
Há moléculas que apresentam hidroxilas ligadas a carbonos bem parecidas com os álcoois no entanto não são álcoois.
O fenol possui uma hidroxila (OH) ligada diretamente ao carbono insaturado, do anel benzênico e portanto não é um álcool. Observe o exemplo.

A Classificação Dos Álcoois
A Classificação Quanto ao Número de Hidroxilas
Monoálcoois
Os monoálcoois possuem somente uma hidroxila (OH) na sua molécula.
Álcool metílico

Álcool etílico

Álcool propílico
Álcool isopropílico
Observe que o álcool é o mesmo, não mudou nada representativamente, apenas a forma de escrever a cadeia carbônica foi colocada diferente, a hidroxila continua no carbono 2.

Diálcoois
Os diálcoois possuem duas hidroxilas na sua estrutura molecular.
Etanodiol
Os diálcoois possuem duas hidroxilas na sua estrutura molecular.
Etanodiol

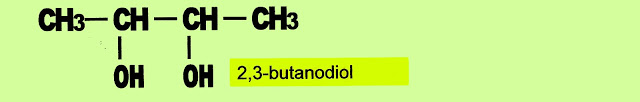
2,3-butanodiol

Triálcoois
Os triálcoois são álcoois com três hidroxilas na sua estrutura molecular. Exemplo.
Propanotriol

O propanotriol ou glicerina é utilizado nos panetones para deixa-los mais fofinhos e úmidos.
Poliálcool
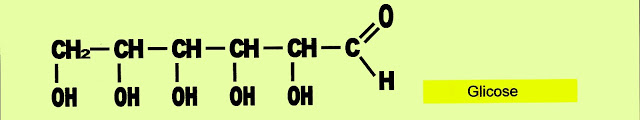
O poliálcool possui várias hidroxilas na sua estrutura molecular. Exemplo.
Glicose
Glicose

A Classificação Dos Álcoois de Acordo Com a Posição da Hidroxila na Molécula
a) Álcoois Primários
Os álcoois primários possuem em sua estrutura molecular a hidroxila ligada ao carbono da extremidade da cadeia, ou seja no carbono primário. Exemplo.

b) Álcoois Secundários
Nos álcoois secundários a hidroxila está ligada no carbono secundário. Exemplo: o 2-butanol ou álcool isobutílico, ou o 2-propanol ou álcool isopropílico.


c) Álcoois Terciários
Nos álcoois terciários a hidroxila está ligada diretamente no carbono terciário.

Álcoois de Cadeia Cíclica

Álcoois Com Anéis Benzênicos
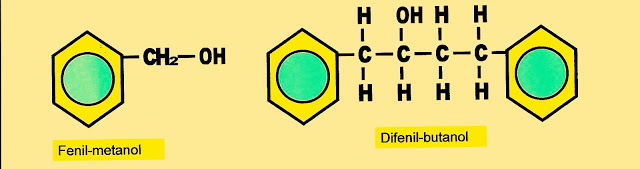
Fenil-metanol e 1,4-difenil-2-butanol
Fenil-metanol e 1,4-difenil-2-butanol

Solubilidade de Alguns Álcoois em Água
Metanol é muito solúvel em água.
Etanol é muito solúvel em água.
Propanol é muito solúvel em água.
O butanol é apenas 8% solúvel em água.
O pentanol é solúvel em água apenas 2,2%.
o hexanol é solúvel em água apenas 0,6%.
Utilização Dos Álcoois
O Que é Álcool Anidro?
Álcool Anidro é álcool sem água mesmo que seja residual. É álcool etanol ou álcool etílico 100% puro. É obtido industrialmente destilando o álcool comum com benzeno. O benzeno arrasta consigo os 4 % de água existente no álcool comum. O álcool anidro é utilizado misturado à gasolina no abastecimento de veículos.
O Uso do Metanol
O metanol ou carbinol ou álcool metílico, álcool de madeira, é utilizado como combustível para veículos. Sua combustão é completa com alto rendimento energético. Os veículos movidos a metanol emitem menos restos de combustíveis não queimados, no entanto mesmo como combustível de automóveis é capaz de produzir o metanal que pode dar origem a câncer.
Uso do Etanol
O etanol anidro é utilizado como combustível para veículos misturado á gasolina, ou puro 100% anidro ou absoluto.
O etanol pode ser usado também como solvente e está contido nos perfumes, loções, desodorantes e tem sua aplicação na limpeza doméstica em geral.
- nos hospitais como anti-séptico esterilizante.
- na produção de plásticos.
- na fabricação do etileno, éter e acetileno.
O etanol está presente nas bebidas destiladas em geral como uísque, vodca, aguardentes em geral, nas bebidas fermentadas e depois destiladas, como os conhaques, vinhos, ou ainda temos o álcool que compõe a champanha que é fermentado no próprio recipiente, e os das cervejas.

A foto ao lado mostra a cana-de-açúcar- da família Poaceae, gênero saccharum - Saccharum officinarum, é uma gramínea, principal fonte da qual se extrai o caldo da cana utilizado na preparação do açúcar sacarose e álcool etanol. Observe as touceiras da que foi retirada as palhas para uma melhor visualização. Nas propriedades agrícolas ela se apresenta com as palhas protegendo os colmos até o momento da colheita. Nesta fase visualizada aqui, ela ainda está em crescimento, não está madura. Irá crescer o dobro ou o triplo do tamanho apresentado na foto, até chegar ao ponto de maturação, quando o teor de açúcar atingir aproximadamente 13 % da massa do colmo, é que será colhida.
Ao fundo atrás dos frascos observamos uma caixa de lâminas para microscopia.
Observação:
A foto ao lado mostra a cana-de-açúcar- da família Poaceae, gênero saccharum - Saccharum officinarum, é uma gramínea, principal fonte da qual se extrai o caldo da cana utilizado na preparação do açúcar sacarose e álcool etanol. Observe as touceiras da que foi retirada as palhas para uma melhor visualização. Nas propriedades agrícolas ela se apresenta com as palhas protegendo os colmos até o momento da colheita. Nesta fase visualizada aqui, ela ainda está em crescimento, não está madura. Irá crescer o dobro ou o triplo do tamanho apresentado na foto, até chegar ao ponto de maturação, quando o teor de açúcar atingir aproximadamente 13 % da massa do colmo, é que será colhida.
Álcool Etanol - Cetona na Análise Bacterioscópica
O álcool acetona é preparado por laboratórios químicos especializados, de onde se pode adquirir. Pode ainda ser preparado "in lócus"; no próprio laboratório clínico, a partir dos produtos químicos adquiridos puros, da seguinte maneira: a mistura é feita com proporções mais ou menos 50% de etanol e mais ou menos 50% de acetona, ambos com padrões PA.
O álcool acetona é utilizado no laboratório de análises clínicas para descoloração de lâminas de exames bacterioscópicos de Gram.
A coloração de Gram é feita da seguinte forma: numa lâmina de esfregaço, já preparada antecipadamente com uma secreção já seca, que fora coletada de um paciente do qual se suspeita ter infecção bacteriológica, coloca-se o corante cristal violeta de genciana preenchendo toda a superfície da lâmina, deixa-se o corante penetrar nas estruturas as serem coradas por um minuto, logo após esse tempo, sobre a lâmina coloca-se uma solução diluída de lugol, deixa o lugol reagir com o cristal violeta por mais um minuto ocorrendo a fixação da cor. Logo a seguir, descora-se a lâmina, ou seja, as estruturas Gram negativas, com o álcool acetona. A seguir cobre a lâmina com safranina por um minuto. Se a bactéria presente no esfregaço for Gram positiva o corante violeta de genciana atravessa a membrana e penetra no interior das células. Ao ser descorada, a lâmina, apresenta as estruturas observadas pela microscopia óptica, apenas as bactérias Gram positivas que absorveram o corante, e que permanecem com a coloração violeta escuro, sendo assim diagnosticadas. Se a bactéria for Gram negativa ao lavar a lâmina com álcool acetona, este retira todo o corante violeta que não penetrou no interior da célula que fica totalmente descorada e a parede celular tomará o corante safranina de cor vermelha.

A coloração de Gram é feita da seguinte forma: numa lâmina de esfregaço, já preparada antecipadamente com uma secreção já seca, que fora coletada de um paciente do qual se suspeita ter infecção bacteriológica, coloca-se o corante cristal violeta de genciana preenchendo toda a superfície da lâmina, deixa-se o corante penetrar nas estruturas as serem coradas por um minuto, logo após esse tempo, sobre a lâmina coloca-se uma solução diluída de lugol, deixa o lugol reagir com o cristal violeta por mais um minuto ocorrendo a fixação da cor. Logo a seguir, descora-se a lâmina, ou seja, as estruturas Gram negativas, com o álcool acetona. A seguir cobre a lâmina com safranina por um minuto. Se a bactéria presente no esfregaço for Gram positiva o corante violeta de genciana atravessa a membrana e penetra no interior das células. Ao ser descorada, a lâmina, apresenta as estruturas observadas pela microscopia óptica, apenas as bactérias Gram positivas que absorveram o corante, e que permanecem com a coloração violeta escuro, sendo assim diagnosticadas. Se a bactéria for Gram negativa ao lavar a lâmina com álcool acetona, este retira todo o corante violeta que não penetrou no interior da célula que fica totalmente descorada e a parede celular tomará o corante safranina de cor vermelha.
A foto a esquerda mostra um frasco com álcool acetona preparado, no laboratório clínico e um frasco adquirido no comércio com o conteúdo já pronto para uso.
Ao fundo atrás dos frascos observamos uma caixa de lâminas para microscopia.
Observação:
O manuseio da acetona ?in natura?, deve ser feito em ambiente adequado, pois se trata de um produto com grau de toxicidade expressiva. Também é aconselhável seguir as normas técnicas para manipulação orientada pela ANVISA, ou a orientação recomendada pelo próprio fabricante.
Uso do Etano-glicol - Glicerina
O etano-glicol é utilizado na produção de polímeros e de nitroglicerina. A glicerina também faz parte dos ácidos graxos (gorduras) os seres biológicos.
- como solvente
- como solvente, plastificante e lubrificante.
- como agente adoçante.
- como agente adoçante.
- na produção de cosméticos.
- na produção de tintas e resinas tipo poliéster.
- na produção de tintas e resinas tipo poliéster.
Tem sua aplicação na produção de trinitroglicerina um potente explosivo.
O propanotriol ou glicerina é utilizado nos panetones para deixa-los mais fofinhos e úmidos.
Utilização do Xilitol
O xilitol é outro tipo de substância que está inserida no grupo dos álcoois, também é utilizado como açúcar, pois evita as cáries dentárias, é adicionado em xaropes, em balas e gomas de mascar especialmente por não interferir na saúde dentária.
O propanotriol ou glicerina é utilizado nos panetones para deixa-los mais fofinhos e úmidos.
Uso do Álcool Isopropílico ou Isopropanol ou 2-butanol
O álcool isopropílico pode ser encontrado facilmente no mercado em conteúdo que varia desde um simples pequeno frasco de 50 mL, até em embalagens do tipo barril de 150 litros em grandes quantidades, com uma variedade de nomes comerciais.
Esse álcool se mistura bem com a água, no entanto no estado puro é muito inflamável. Quanto a sua toxicidade se dá pelo contato direto com o líquido ? in natura?, ou por aspiração de seus gases.
É empregado na limpeza doméstica, estendendo essa aplicabilidade para os objetos de metais. Na industria é aplicado como solvente de resinas, de óleos, gorduras, alcalóides, acetatos de celulose, nitrocelulose. Pode também ser utilizado nas preparações de tintas; tem seu emprego na preparação de tinta para impressão numa proporção de 2% na fórmula, nos vernizes, também tem sua participação na industria de eletroeletrônicos, serve ainda como removedor, se emprega na perfumaria e nos cosméticos e como medicamento está na forma de soluções antissépticas de uso externo. Além disso está contido em fórmulas de produtos farmacêuticos, da acetona, do peróxido de hidrogênio e metil-isobutil-cetona, no nitrato isopropílico. O isopropanol é ainda utilizado também como agente flavorizante.
Aplicação do Álcool isobutílico
Nome em Inglês; Isobutyl alcohol
Esse álcool solúvel em água e éter pode Pode ser adquirido em embalagens de 2,5L, 25 L, e tambor de 190 L. Pode ser utilizado na fabricação de essências de frutas, perfumes, síntese de substâncias orgânicas, podendo também ser aplicado como solvente de várias substâncias, é um bom removedor de tintas, porém é relativamente tóxico.
A Utilização do Sorbitol - hexano-hexol
O sorbitol também está inserido no grupo dos álcoois, no entanto também é um açúcar utilizado nos cremes dentais, é o responsável pelo sabor doce desses cremes. sua utilização pelo organismo não é total, e é eliminado antes de ser totalmente metabolizado pelo organismo. Provoca diarreias se ingerido em quantidade acima do limite que o organismo consegue suportar sem reagir.
A Utilização do Sorbitol - hexano-hexol
O sorbitol também está inserido no grupo dos álcoois, no entanto também é um açúcar utilizado nos cremes dentais, é o responsável pelo sabor doce desses cremes. sua utilização pelo organismo não é total, e é eliminado antes de ser totalmente metabolizado pelo organismo. Provoca diarreias se ingerido em quantidade acima do limite que o organismo consegue suportar sem reagir.
Utilização do Xilitol
O xilitol é outro tipo de substância que está inserida no grupo dos álcoois, também é utilizado como açúcar, pois evita as cáries dentárias, é adicionado em xaropes, em balas e gomas de mascar especialmente por não interferir na saúde dentária.
O Álcool no Organismo Humano
Cabe aqui servir de alerta, especialmente para o jovem que está em transição, todo entusiasta de suas possibilidades, na confiança de sua própria capacidade de resistência ás bebidas alcoólicas. Na primeira vez, a primeira dose, são novas descobertas, novas sensações, E a euforia no convívio das amizades, o calor, o rubor, a diminuição da inibição, a predisposição às novas aventuras, é um embarcar rumo ao desconhecido. Há!!! Isso é uma boa! (...).
É claro que se tratando do álcool e o risco á saúde, há também a implicação de uma série de fatores, entre os quais os mais evidentes são: o tempo de exposição a droga, a quantidade, e a frequência de ingestão.
Não se tratando dos alcoólatras inveterados, que nesse caso o assunto deve ser tratado separadamente de outra forma, na pessoa normal, de início para se fazer qualquer análise, primeiramente deve se levar em conta, que a ação da droga depende de cada indivíduo, do estado físico e da sua personalidade. Especialmente para o jovem forte e sadio que está a fim de curtir, nas primeiras doses a sensação de euforia predomina nos encontros sociais. Ao avançar as horas e o aumento das doses ingeridas, em sequência, aquela sensação agradável proporcionada de início, pode começar a desaparecer, e toma lugar a alteração do humor, que também varia proporcionalmente de indivíduo para indivíduo e da sua predisposição em relação ao álcool. Nesse ponto, se a pessoa não limitar a própria ingestão da bebida alcoólica, se torna instável emocionalmente, somado a diminuição da sua atenção e dos seus reflexos ao que está a sua volta, em evidência essa interferência neural, ou neurológica, evolui para uma descoordenação psico-motora corporal total. O indivíduo antes sociável, agora se torna alienado ao próprio ambiente.
Passado o primeiro período, inicia-se outro, de 8 a 12 horas, vem a "ressaca", nesse tempo quase todo o álcool e seus metabólitos, ou as substâncias tóxicas, já foram eliminados do organismo do indivíduo. No entanto, além de desidratação que o indivíduo apresenta nessa fase, exames laboratoriais revelam a diminuição do Ph do sangue, (acidose), aumento do lactato, um promovedor da dor no corpo, e a presença de outras substâncias, os corpos cetônicos, e a análise clínica revela ainda, há a ocorrência de ácidos graxos livres presentes na corrente sanguínea. Os sintomas apresentados agora pela pessoa, consiste em um mal estar geral que é caracterizado principalmente por: dor de cabeça, náusea, tremores e vômitos.
Ao ser ingerido, a absorção do álcool se dá nas paredes do estômago. Quando cheio a absorção nessa região é menor, outra parte é absorvida no cólon, e a maior parte é absorvida no intestino delgado. Daí pela corrente sanguínea se difunde para todo o corpo. Indo para os pulmões, rins, até ao cérebro, atuando no sistema nervoso, onde influencia de maneira drástica. A eliminação pode acontecer in natura na urina, pelos pulmões juntamente com o ar expirado. No entanto a maior parte é essencialmente metabolizado no fígado via enzima álcool desidrogenase IB (class I), ou beta polipeptídio (ADH1B), em gás carbônico (CO2), água (H2O) e acetaldeido, O acetaldeido é muito instável formador de estruturas com radicais livres que são tóxicos que nem mesmo os antioxidantes como o ácido ascórbico (Vitamina C) ou a Vitamina B1 (tiamina) é capaz de metabolizá-los. Na sequência dos fatos, no organismo, duas enzimas, uma localizada no citosol e outra mitocondrial, ambas; são capazes de metabolizar o acetaldeído. Essas enzimas que convertem o acetaldeido em ácido acético, são chamadas de aldeído desidrogenase. São as que possibilitam a retirada do acetaldeído do organismo, transformando-o em ácido acético, através de uma série de biotransformações, podendo gerar energia, ou transformando-as em gordura, que é armazenada como tecido adiposo. Contudo se a ingestão do álcool for em excesso, prolongado e contínuo, nem todo acetaldeido consegue ser metabolizado, nesse caso, pela ação tóxica dessa substância, ocorre danos ás estruturas das células neuronais, embrionárias e consequentemente causa danos, no caso de grávida; para a formação dos nascituros, para o próprio fígado e os rins do usuário, onde causa danos muitos sérios. Os produtos relacionados ao metabolismo do álcool, como as cetonas e pequena parte do acetaldeido, pode voltar ao sistema circulatório, ser filtrado nos rins e eliminados na urina. A ingestão contínua do álcool pode acarretar ainda, forte acidez localizadas, proporcionando lesões do estomago que se estende para os intestinos chegando até o reto, com sangramento. Nesse caso, o indivíduo pode apresentar hemorragia retal.
Os efeitos nocivos do álcool se mostra também nas dependentes grávidas, nestas; pode ocorrer a síndrome do alcoolismo fetal, ou levar a acontecer as malformações congênitas que conduz às diversas causas de extrema consequências, entre as quais estão: a microcefalia que é a diminuição do tamanho do cérebro do bebê, esta deformação inicia-se na fase fetal e permanece durante toda a existência do portador, a caixa craniana e o cérebro são pequenos em relação ao rosto que é grande. Acontecem outras anomalias como as faciais (SFA) que estão relacionadas ao alcoolismo gestacional, por exemplo; indivíduos que apresentam a falta de sobrancelhas, ou ainda o hipertelorismo ocular, que se trata do afastamento excessivo dos olhos na face, ou ainda a ptose palpebral que consiste em ter a pálpebra superior caída sobre os olhos, essa mesma anomalia pode apresentar o portador com as orelhas baixas, em relação ao conjunto facial normal.
A Nomenclatura Dos Álcoois
Para darmos nomes aos álcoois devemos nos basear sempre na hidroxila, A hidroxila comanda a funcionalidade desse grupo da química orgânica. A nomenclatura reserva para os álcoois a terminação ?ol?.
Numa cadeia acíclica, linear sem ramificações, numera-se a cadeia de carbono iniciando pela extremidade mais próxima da oxidrila (OH). Por exemplo.
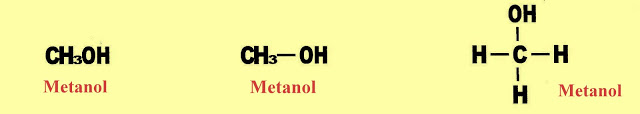
Metanol
Metanol - tem 1 carbono ?met? + ?an? + a terminação ?ol?.

Etanol - tem 2 carbonos ?et? + ?an? + a terminação ?ol?.

Propanol
Propanol - tem 3 carbonos na cadeia ?prop? + ?an? + a terminação ?ol?.

Butanol
Butanol - tem 4 carbonos na cadeia ?but? + ?an? + a terminação ?ol?.

Pentanol
Pentanol - tem 5 carbonos na cadeia ?pent? + ?an? + a terminação ?ol?.

Hexanol ou 1 hexanol
Hexanol, tem 6 carbonos na cadeia ?hex? + ?an? + a terminação ?ol?
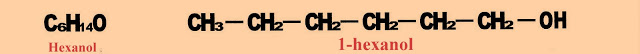
3-hexanol
No 3-hexanol, a posição da hidroxila está no carbono 3 dos seis carbonos da cadeia principal ?hex? + ?an? + a terminação ?ol?
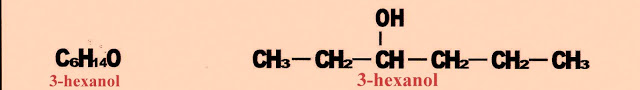
Glicerina ou glicerol ou 1,2,3-propanotriol

O propanotriol é adicionado nas massas dos panetones, principalmente os industrializados, para reter a umidade ou seja como umectante, para deixar a massa com consistência macia e não resseque.
Nomes Para Álcoois em Que a Hidroxila Não Está no Carbono Terminal, Mas no Carbono Intermediário
Álcool isopropílico
Propanol-2
Propanol-2
A hidroxila está ligada no carbono secundário e é chamado de álcool isopropílico ou 2-propanol.

Álcool isobutílico, nome usual.
2-butanol
2-butanol
A hidroxila está ligada ao carbono 2 da cadeia de 4 carbonos, recebe o prefixo ?but? + a terminação "ílico".

Álcool terci-butílico
2-metil-2-propanol
2-metil-2-propanol
A hidroxila está ligada no carbono 2, que é terciário e está ligado a outros três carbonos. Nesse mesmo carbono há ligado um radical metil, que forma a estrutura molecular de 4 carbonos.


Nomenclatura Dos Álcoois de Cadeia Ramificada
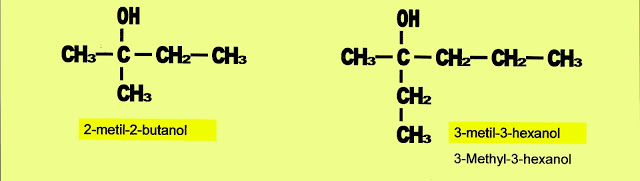
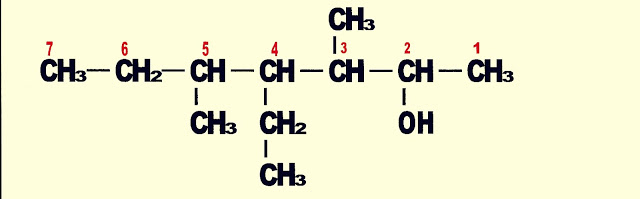
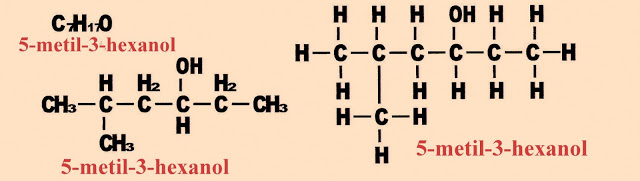
5-metil-3-hexanol
Primeiramente conta-se o número de carbonos da cadeia principal começando pelo lado da cadeia em que a hidroxila estiver mais próxima da extremidade. Depois começa a nomeação pelo carbono em que o radical metil está inserido, em seguida coloca-se o número do carbono em que a hidroxila está inserida, o número total de carbonos da cadeia e finalmente a terminação ol.


4-etil-3,5-dimetil-2-heptanol

Álcoois Com Cadeia Carbônica Cíclica
Ciclo-hexanol
Observe que a hidroxila está ligada diretamente no carbono da cadeia cíclica saturada.
Ciclo-hexanol
Observe que a hidroxila está ligada diretamente no carbono da cadeia cíclica saturada.

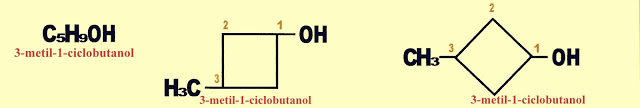
3-metil-1-ciclobutanol

Estes álcoois apresentam suas cadeias carbônicas como duplas ou triplas ligações entre seus carbonos.
2-metil-2-buten-1-ol (IUPAC)

Nomenclatura Dos Álcoois de Kolbe
Na nomenclatura de Kolbe seria formada a partir do metanol, a hidroxila está ligada ao carbono saturado formando o radical que é chamado de carbinol.
Carbinol

Nome oficial: metanol.
Nome usual: álcool metílico.
Nome segundo Kolbe: carbinol.

Nome oficial: etanol.
Nome usual: álcool etílico.
Nome segundo Kolbe: metil-carbinol.

Nome usual: álcool terci-butílico
Nome segundo Kolbe: trimetil-carbinol.

Isomeria Que Acontece Com os Álcoois
Isomeria Funcional ? Álcool-Éter
A isomeria funcional é aquela em que a formula molecular, massa molecular, são iguais, mas os grupos funcionais são diferentes. Por exemplo, a isomeria que acontece com um álcool e um éter.

Isomeria de Posição
A Isomeria de posição acontece com o 1-butanol e o 2-butanol. A hidroxila está em posição diferente em cada molécula.

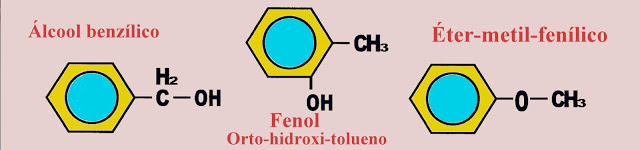
Isomeria Álcool aromático Fenol e Éter
Álcool benzílico, orto-hidroxi-tolueno, éter-metil-fenílico

Reações Dos Álcoois
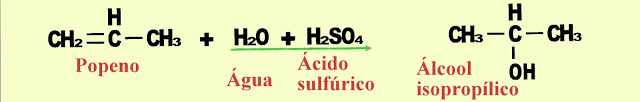
Produção de um álcool a partir de um alceno
O propeno mais água mais ácido sulfúrico forma o álcool isopropílico.

Produção de um Álcool a Partir do Carbono e Água
O gás monóxido de carbono (CO) mais duas moléculas de gás hidrogênio (H2) com os catalisadores trióxido de cromo (CrO3) e zinco (Zn), mais a temperatura de 400ºC e 200 atmosferas de pressão, origina o metanol (CH3OH). Observemos a equação dessa transformação.

A Produção do Metanol a Partir do Metano
O gás metano reage com o oxigênio a 500 ºC de temperatura e 15 atmosferas de pressão e catalisador, resulta no etanol. A equação da transformação é:

Produção de Metanol a Partir do Etileno
O etileno reage com água em meio ácido e se transforma em álcool etílico.

A Produção de Vinagre a Partir do Vinho
O vinho que contém álcool, oxida esse álcool presente em sua composição, transformando-o em vinagre. Para fazer vinagre de vinho, basta adicionar bactérias Acetobacter Aceti e deixar o vinho fermentar até azedar, nessa transformação o etanol reage com o o oxigênio (O2) transformando-se no ácido acético, que contribui na formação desse vinagre numa proporção de 4 a 6%. É importante saber que na composição final do vinagre, deve restar resquícios de álcool. Caso todo o álcool seja consumido, as próprias bactérias passam a degradar o ácido acético do composto, prejudicando a qualidade do vinagre. Há outras técnicas como a que usa leite para azedar o vinho.
A Produção do Etanol a Partir da Cana de Açúcar
Existem vários processos tecnológicos bem avançados para a produção do etanol industrialmente. Resumidamente pode ser descrito um dos métodos com característica técnica bem comum, para a produção do açúcar e do etanol em grande escala comercial.
Na fabricação do álcool etanol, a primeira fase, é a da lavagem e moagem da cana de açúcar, a partir da moagem, o bagaço da cana resultante pode ser queimado para a produção de energia térmica na própria industria, ou destinado para outro aproveitamento, como na fabricação de ração animal ou adubo orgânico. No próximo passo, o caldo obtido passa para tanques aonde acontece o processo de sulfitação ou seja; a adição de dióxido de enxofre, substância que não pode exceder 10 mg/L, na concentração desse suco obtido. Na sequência o conteúdo é passado para o tanque seguinte e aí é adicionado a substância que provoca a floculação das partículas sólidas em suspensão no líquido, o conteúdo recebe certa porcentagem de cal, ou bicarbonato de cálcio ou bicarbonato de sódio (...), que provoca a floculação desejada removendo parte de substâncias indesejáveis. No próximo passo o caldo da cana, passa por um processo de floculação e e remoção de partículas que são descartadas num campo para resíduos, o conteúdo é passado para outro recipiente aonde se completa o processo de clareamento, e posterior filtração do caldo. No próximo passo, o caldo da cana, passa por um processo de floculação e e remoção de partículas que são descartadas num campo próprio para resíduos, o líquido é passado para outro tanque, lá acontece o processo de clareamento, e posterior filtração. Na sequência, ao chegar á próxima etapa, nesse outro tanque, sofre aquecimento moderado acontecendo a evaporação das substâncias liquefeitas com engrossamento do caldo tornando-o mais viscoso, a partir daí ha a passagem mais uma vez para outro recipiente, onde sofre fervura até o conteúdo obtido estar próximo a cristalização como açúcar já pronto, na sequência ocorre a centrifugação e secagem até tomar a forma de cristais de açúcar como nós conhecemos e pode ser comercializado.
A Produção de Álcool a Partir do Açúcar
C12H22O11 + H2O ---- Invertase ----- C6H12O6 + C6H12O6
Sacarose Água Enzima Glicose Frutose
Glicose
a ---- ---------- Zimase ------ Fermentação--- Álcool 96%
Frutose enzima responsável Mosto
pelo desdobramento
do açúcar em álcool
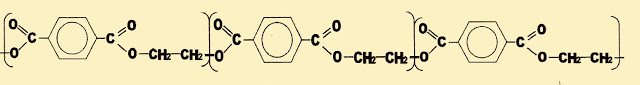
Reciclagem do Politereftalato de Etileno
O álcool etanoglicol ou etilenoglicol entra na composição do plástico politereftalato de etileno, que pode ser reaproveitado sendo transformado novamente em etilenoglicol pela hidratação do politereftalato pela reação:
No entanto o etilenoglicol também pode ser produzido pela reação do óxido de etileno com água com auxílio de catalisador.

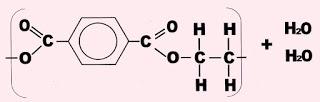
Os monômeros do polietilenotereftalato se unem para formar o polímero PET, ou fibras do poliéster.
Exercícios

Bibliografia
A Produção de Álcool a Partir do Açúcar
Para a fabricação do álcool, o produto final após ser centrifugado não passa necessariamente pelo processo de secagem, mas vai diretamente para tanques de fermentação aonde permanece por algum tempo, para fermentar por meio das leveduras chamadas de Sacharomyces cerevisae que possuem a enzima chamada de invertase, que quebram o açúcar sacarose (C12H22O11) em dois outros açúcares, a glicose (C6H12O6) e frutose C6H12O6), que pela ação de outra enzima, a zimase que desdobra esses açúcares, na produção do álcool.
Após esse período, a composição ou mistura é aquecida até o ponto de evaporação do álcool e daí por diante passa pela destilação fracionada e no próximo recipiente ainda passa por mais um processo de retificação do produto para a obtenção do álcool 96%, e daí para a coluna de esvaziamento, para ser distribuído para o mercado, ou segue para a coluna de desidratação para obtenção do etanol combustível 100% puro, daí o produto final segue para os distribuidores do combustível para os veículos automotores.
Após esse período, a composição ou mistura é aquecida até o ponto de evaporação do álcool e daí por diante passa pela destilação fracionada e no próximo recipiente ainda passa por mais um processo de retificação do produto para a obtenção do álcool 96%, e daí para a coluna de esvaziamento, para ser distribuído para o mercado, ou segue para a coluna de desidratação para obtenção do etanol combustível 100% puro, daí o produto final segue para os distribuidores do combustível para os veículos automotores.
Processo Simplificado da Produção de Álcool
C12H22O11 + H2O ---- Invertase ----- C6H12O6 + C6H12O6
Sacarose Água Enzima Glicose Frutose
Glicose
a ---- ---------- Zimase ------ Fermentação--- Álcool 96%
Frutose enzima responsável Mosto
pelo desdobramento
do açúcar em álcool
Reciclagem do Politereftalato de Etileno
O álcool etanoglicol ou etilenoglicol entra na composição do plástico politereftalato de etileno, que pode ser reaproveitado sendo transformado novamente em etilenoglicol pela hidratação do politereftalato pela reação:
No entanto o etilenoglicol também pode ser produzido pela reação do óxido de etileno com água com auxílio de catalisador.

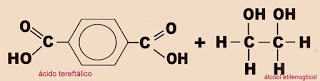
A formação do politereftalato a partir do ácido tereftálico e do álcool etilenoglicol.
Na reação, o hidrogênio das carboxilas do ácido tereftálico se unem ás hidroxilas do álcool e saem como água.

Monômero do Polietilenotereftalato(PET)


Exercícios
1) Podemos definir os álcoois como:
a) Álcoois podem ser definidos como substâncias que possuem o radical funcional o cátion H+ ou o hidrônio H3O+.
b) Álcoois são hidrocarbonetos insaturados cuja cadeia carbônica aberta é a principal e possui uma única dupla ligação entre seus carbonos.
c) Álcoois são compostos orgânicos contendo uma ou mais hidroxilas (OH) ligada (s) diretamente a átomo (s) de carbono (s) saturado (s).
d) Álcoois são compostos orgânicos com o radical carbonila, ou aldoxila, carbono ligado por dupla ligação a um oxigênio e por uma única ligação a um hidrogênio.
e) Ácidos carboxílicos são compostos orgânicos de caráter ácido fraco, que possuem na sua estrutura molecular um ou mais radical, a carboxila (COOH).
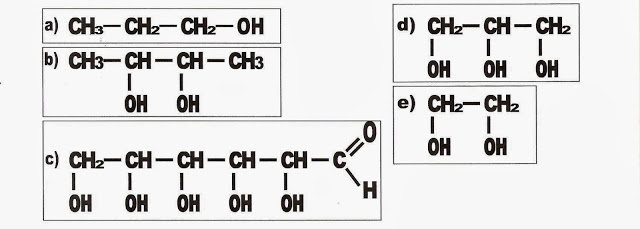
2) Das moléculas apresentadas abaixo é um álcool apenas a alternativa.

a) ( ) b) ( ) c) ( ) d) ( ) e) ( )
3) De acordo com a classificação dos álcoois conforme o número de hidroxilas podemos considerar um triálcool apenas a alternativa:

a) ( ) b) ( ) c) ( ) d) ( ) e) ( )
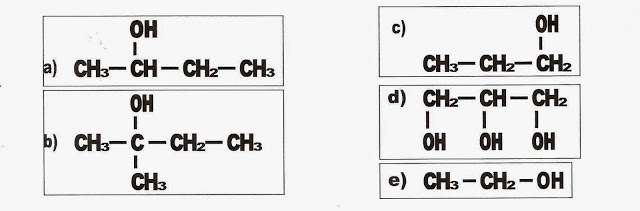
4) De acordo com a classificação dos álcoois em primários, secundários e terciários, assinale apenas a molécula que representa um álcool terciário.

a) ( ) b) ( ) c) ( ) d) ( ) e) ( )
5) O álcool isobutílico, nome usual, o mesmo que álcool terci-butílico. Esse álcool é solúvel em água e éter. É comercializado em embalagens de 2,5L, 25 L, e tambor de 190 L. Pode ser utilizado na fabricação de essências de frutas, perfumes, síntese de substâncias orgânicas, podendo também ser aplicado como solvente de várias substâncias, é um bom removedor de tintas. A hidroxila na molécula está ligada:
a) no carbono 2, que é terciário.
b) no carbono 1, que é terciário.
c) no carbono 3, que é terciário.
d) no carbono 2, que é secundário.
e) no carbono 1, que é secundário.
Bibliografia
Martha Reis Marques da Fonseca. Química, Meio Ambiente, Cidadania, Tecnologia, 1a edição, Editora FTD, volume 3. São Paulo - 2010.
Tito e Canto. Química na Abordagem do Cotidiano. 2a edição. Volume 3. Editora Moderna. São Paulo - SP.
Usberco, Salvador Química Orgânica. 2a edição, volume 3. Editora Saraiva. São Paulo - SP
Ricardo Feltre. Química Orgânica, 6a edição, volume 3. Editora Moderna. São Paulo - 2004
Usberco, Salvador Química Orgânica. 2a edição, volume 3. Editora Saraiva. São Paulo - SP
Ricardo Feltre. Química Orgânica, 6a edição, volume 3. Editora Moderna. São Paulo - 2004
Ethanol metabolism ? Wikipedia, the free encyclopedia
en.wikipedia.org/.../Ethanol_meta...
Produção de Etanol de cana-de-açúcar_carlos
www.inovação.unicamp.br/.../workshop-etanol_carlos-...
Processamento da cana-de-açúcar
www.agencia.cnptia.embrapa.br/.../cana-de-açúcar/.../c...
Os efeitos do álcool no organismo humano ? síndrome fetal do...
Proavirtualg30.pbworks.com/.../...
loading...
- Funções Orgânicas E Nomeclatura
Dentro da química orgânica existem as funções orgânicas (compostos ôrganicos de características químicas e físicas semelhantes). Existem muitas funções, sendo as mais comuns:· Hidrocarbonetos (Alcanos, Alcenos, Alcinos, Alcadienos, Alcadiinos,...
- O Álcool Do Nosso Dia A Dia
Tatiane dos Santos Olá amigos do blog! O assunto de hoje é bastante conhecido por todos, o álcool ou quimicamente falando etanol, ou melhor, álcool etílico!O etanol é um composto orgânico obtido na maioria das vezes da cana de açúcar, porém...
- ?as Bebidas Fortes Fazem Os Homens Fracos?
Bolsista: Alessandro R. Barbosa Oi seguidores e amigos do QUIPIBID! Hoje atualizamos nossa coluna de atualidades com uma reportagem do portal G1, sobre a Europa ser a região líder no...
- Oxidação Do álcool Com Dicromato De Potássio.
OXIDAÇÕES DE ÁLCOOIS COM DICROMATO DE POTÁSSIO Fácil e ilustrativo Embora façamos muita menção por aqui ao emprego do dicromato de potássio (K2Cr2O7) como agente oxidante em reações inorgânicas (que é a base do método de titulação...
- Propriedades Químicas Dos Alcoóis
Os compostos pertencentes a esta função química são muito reativos, devido a presença da hidroxila ou oxidrila. O hidrogênio confere um leve caráter ácido ao grupo oxidrila, sendo, portanto mais reativos que os hidrocarbonetos, devido a polaridade...
